Exubera za liječenje dijabetesa
Robna marka: Exubera
Generičko ime: humani inzulin
Oblik doziranja: prašak za inhalaciju
Sadržaj:
Opis
Klinička farmakologija
Kliničke studije
Indikacije i upotreba
kontraindikacije
Upozorenja
Mjere opreza
Interakcije s lijekovima
Nuspojave
predoziranje
Doziranje i primjena
Kako se isporučuje
Exubera, humani inzulin [rDNA porijeklo] Podaci o pacijentu (na običnom engleskom)
Opis
Exubera® sastoji se od blistera koji sadrže prašak za inhalaciju ljudskog inzulina, koji se daje primjenom Exubera® Inhalator. Blisteri Exubera sadrže ljudski inzulin proizveden rekombinantnom DNK tehnologijom koristeći nepatogeni laboratorijski soj Escherichia coli (K12). Kemijski, ljudski inzulin ima empirijsku formulu C257H383N65O77S6 i molekulska masa 5808. Ljudski inzulin ima sljedeću sekvencu primarnih aminokiselina:
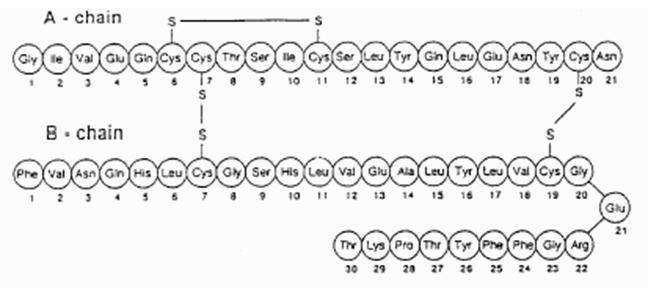
Exubera (humani inzulin [rDNA porijeklo]) Inhalacijski prah je bijeli do gotovo bijeli prah u blisteru s jediničnom dozom (ispunite masu, vidjeti tablicu 1). Svaki blister jedinice Exubera s jednom dozom sadrži dozu inzulina od 1 mg ili 3 mg (vidjeti tablicu 1) u a homogena formulacija praška koja sadrži natrijev citrat (dihidrat), manitol, glicin i natrij hidroksid. Nakon što je blister Exubera ubačen u inhalator, pacijent pumpa ručicu inhalatora i zatim pritisne gumb, uzrokujući da se mjehur probije. Prah za inhalaciju inzulina se zatim raspršuje u komoru, omogućavajući pacijentu da inhalira aerosolizirani prah.
Pod standardiziranim in vitro uvjetima ispitivanja, Exubera isporučuje specifičnu emitiranu dozu inzulina iz usnika inhalatora (vidjeti tablicu 1). Djelić ukupne mase čestica emitira se u obliku sitnih čestica sposobnih doprijeti do dubokog pluća. U blisteru se može zadržati do 45% od 1 mg sadržaja blistera i do 25% od 3 mg.
Tablica 1: Nomenklatura i podaci doze
| Ispunite misu (mg praška) |
Nominalna doza (mg inzulina) |
Emitirana doza*,†(mg inzulina) |
Doza sitnih česticac,†(mg inzulina) |
|---|---|---|---|
| |||
| 1.7 | 1.0 | 0.53 | 0.4 |
| 5.1 | 3.0 | 2.03 | 1.0 |
Stvarna količina inzulina koja se dostavlja u pluća ovisit će o pojedinim čimbenicima bolesnika, kao što je profil protoka inspiracije. In vitro, mjerni podaci emitirane aerosole ne utječu na brzinu protoka iznad 10 L / min.
vrh
Klinička farmakologija
Mehanizam djelovanja
Primarna aktivnost inzulina je regulacija metabolizma glukoze. Inzulin smanjuje koncentraciju glukoze u krvi stimulirajući periferni unos glukoze u skeletne mišiće i masnoću i inhibirajući stvaranje jetrene glukoze. Inzulin inhibira lipolizu u adipocitu, inhibira proteolizu i pojačava sintezu proteina.
farmakokinetika
apsorpcija
Exubera daje inzulin oralnom inhalacijom. Inzulin se apsorbira jednako brzo kao i supkutano primijenjeni brzo djelujući analozi inzulina i brže nego supkutano davani redoviti humani inzulin kod zdravih ispitanika i u bolesnika s dijabetesom tipa 1 ili tipa 2 (vidjeti Slika 1).
Slika 1: Srednje promjene u koncentraciji slobodnog inzulina u serumu (µU / mL) u bolesnika s dijabetesom tipa 2 koji slijede Davanje pojedinačnih doza inhaliranog inzulina iz Exubere (6 mg) i subkutanog redovnog humanog inzulina (18U)
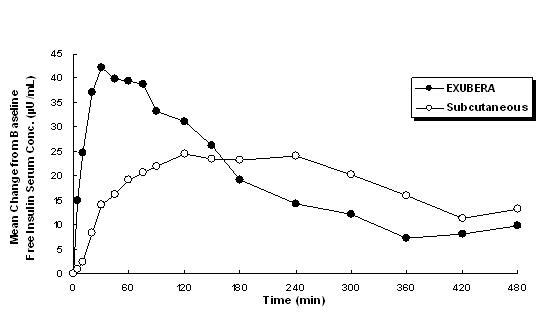
U kliničkim ispitivanjima bolesnika s dijabetesom tipa 1 i 2, nakon inhalacije Exubere, serumski inzulin je dostigao vršnu koncentraciju brže nego nakon potkožne injekcije običnog humanog inzulina, 49 minuta (raspon 30 do 90 minuta) u odnosu na 105 minuta (raspon 60 do 240 minuta), odnosno.
U kliničkim studijama apsorpcija potkožnog redovitog humanog inzulina opadala je s porastom indeksa tjelesne mase pacijenta (BMI). Međutim, apsorpcija inzulina nakon inhalacije Exubera bila je neovisna o BMI.
U studiji na zdravim ispitanicima, sistemska izloženost inzulinu (AUC i Cmax) nakon primjene lijeka Exubera se povećala s dozom u rasponu od 1 do 6 mg, kada se primjenjuje u kombinaciji od 1 i 3 mg mjehurići.
U studiji u kojoj je dozirani oblik tri 1 mg blistera uspoređen s jednim 3 mg blistera, Cmax i AUC nakon primjene tri 1 mg blistera bila su otprilike 30% i 40% veća od one nakon primjene jednog 3 mg blistera (vidjeti DOZIRANJE I UPRAVLJANJE).
Distribucija i uklanjanje
Kako je rekombinantni humani inzulin identičan endogenom inzulinu, očekuje se da će sistemska raspodjela i eliminacija biti isti. Međutim, to za Exubera nije potvrđeno.
farmakodinamiku
Exubera, poput supkutano primijenjenih analoga inzulina brzog djelovanja, ima brži početak aktivnosti snižavanja glukoze od supkutano primijenjenog ljudskog inzulina. U zdravih dobrovoljaca, trajanje aktivnosti snižavanja glukoze za Exubera bilo je usporedivo s potkožno primijenjeni redoviti humani inzulin i dulje od supkutano primijenjenih brzo djelujućih analoga inzulina (vidjeti Slika 2).
Slika 2. Srednja stopa infuzije glukoze (GIR) Normalizirana za GIRmaksimum za svaki subjekt tretman u odnosu na vrijeme u zdravim volonterima
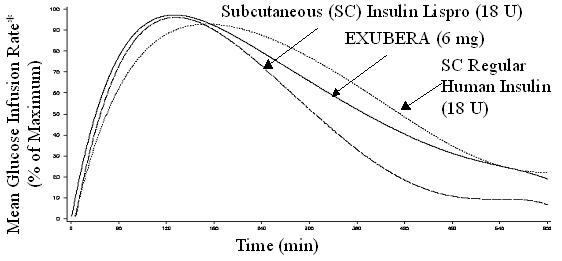
* Određuje se kao količina glukoze infuzirane za održavanje konstantnih koncentracija glukoze u plazmi, normalizirane do maksimalnih vrijednosti (postotak maksimalnih vrijednosti); pokazatelj aktivnosti inzulina.
Kada se Exubera udahne, početak aktivnosti snižavanja glukoze kod zdravih dobrovoljaca događa se u roku od 10-20 minuta. Maksimalni učinak na snižavanje glukoze djeluje otprilike 2 sata nakon udisanja. Trajanje aktivnosti snižavanja glukoze je otprilike 6 sati.
U bolesnika s dijabetesom tipa 1 ili 2, Exubera ima veći učinak snižavanja glukoze u prva dva sata nakon doziranja u usporedbi s subkutano primijenjenim redovitim ljudskim inzulinom.
Varijabilnost aktivnosti lijeka Exubera koja smanjuje glukozu unutar subjekta općenito je uporediva s onim subkutano primijenjenog redovitog humanog inzulina u bolesnika s dijabetesom tipa 1 i 2.
Posebne populacije
Pedijatrijski bolesnici
U djece (6-11 godina) i adolescenata (12-17 godina) s dijabetesom tipa 1, vrijeme za postizanje najveće koncentracije inzulina za Exubera bilo je postiže se brže nego za potkožni redovni humani inzulin, što je u skladu s opažanjima u odraslih bolesnika s tipom 1 dijabetes.
Gerijatrijski bolesnici
Nema očitih razlika u farmakokinetičkim svojstvima Exubere kada se uspoređuju bolesnici stariji od 65 godina i mlađi odrasli pacijenti.
rod
U ispitanika sa i bez dijabetesa nisu primijećene očite razlike u farmakokinetičkim svojstvima Exubere između muškaraca i žena.
utrka
Ispitivanje je provedeno na 25 zdravih kavkaških i japanskih osoba s dijabetesom koji nisu imali dijabetes farmakokinetička i farmakodinamička svojstva Exubera, nasuprot potkožnom ubrizgavanju u redovitog čovjeka inzulin. Farmakokinetička i farmakodinamička svojstva Exubera bila su usporediva između dvije populacije.
gojaznost
Apsorpcija Exubere neovisna je o bolesničkom BMI-ju.
Oštećenje bubrega
Učinak oštećenja bubrega na farmakokinetiku Exubere nije proučen. Pažljiv nadzor glukoze i prilagođavanje doze inzulina mogu biti potrebni bolesnicima s bubrežnom disfunkcijom (vidjeti MJERE OPREZA, Oštećenje bubrega).
Oštećenje jetre
Učinak oštećenja jetre na farmakokinetiku Exubere nije proučen. Pažljiv nadzor glukoze i prilagođavanje doze inzulina mogu biti potrebni u bolesnika s poremećajem jetre (vidjeti MJERE OPREZA).
Trudnoća
Apsorpcija Exubere u trudnica s gestacijskim i pre-gestacijskim dijabetesom tipa 2 bila je u skladu s onom u trudnica s dijabetesom tipa 2 (vidjeti MJERE OPREZA).
Pušenje
U pušača očekuje se da će sistemska izloženost inzulinu Exuberi biti 2 do 5 puta veća nego u nepušača. Exubera je kontraindicirana u bolesnika koji puše ili koji su prestali pušiti manje od 6 mjeseci prije početka terapije Exuberom. Ako pacijent započne ili nastavi pušiti, lijek Exubera mora se odmah prekinuti zbog povećanog rizika od hipoglikemije i mora se koristiti alternativno liječenje (vidjeti KONTRAINDIKACIJE).
U kliničkim istraživanjima Exubere kod 123 bolesnika (od kojih je 69 pušača) pušači su doživjeli brži početak djelovanja za snižavanje glukoze, veći maksimalni učinak i veći ukupni učinak snižavanja glukoze (posebno tijekom prva 2-3 sata nakon doziranja), u odnosu na nepušača.
Pasivni dim cigarete
Suprotno povećanju izloženosti inzulinu nakon aktivnog pušenja, kada je Exubera primijenjena na 30 zdravih dobrovoljnih nepušača nakon 2 sati izlaganja pasivnom dimu cigarete u kontroliranim eksperimentalnim okruženjima, AUC i Cmax inzulina smanjeni su za otprilike 20% i 30%, odnosno. Farmakokinetika Exubere nije ispitivana u nepušača koji su kronično izloženi pasivnom dimu cigarete.
Pacijenti s osnovnim plućnim bolestima
Primjena lijeka Exubera u bolesnika s osnovnom plućnom bolešću, poput astme ili KOPB-a, ne preporučuje se, jer sigurnost i djelotvornost lijeka Exubera u ovoj populaciji nije utvrđena (vidjeti UPOZORENJA). Primjena lijeka Exubera kontraindicirana je kod bolesnika s nestabilnom ili slabo kontroliranom plućnom bolešću, jer su široki varijacije u funkciji pluća koje bi mogle utjecati na apsorpciju Exubere i povećati rizik od hipoglikemije ili hiperglikemija (vidi KONTRAINDIKACIJE).
U farmakokinetičkoj studiji 24 ne-dijabetičara s blagom astmom, apsorpcija inzulina nakon primjene Exubera, u nedostatku liječenja bronhodilatatorom, bila je približno 20% manja od apsorpcije opažene u ispitanika bez astma. Međutim, u istraživanju na 24 subjekta bez dijabetičara s kroničnom opstruktivnom plućnom bolešću (KOPB), sistemska izloženost nakon primjene Exubere bila je približno dvostruko veća od one u normalnih ispitanika bez KOPB (vidi MJERE OPREZA).
Primjena albuterola 30 minuta prije primjene Exubere kod osoba koje nisu dijabetični i s blagom astmom (n = 36) i umjerenom astma (n = 31) rezultirala je srednjim porastom AUC-a i Cmax inzulina između 25 i 50% u odnosu na vrijeme primjene lijeka Exubera (vidjeti MJERE OPREZA).
vrh
Kliničke studije
Sigurnost i djelotvornost lijeka Exubera proučavana je u oko 2500 odraslih pacijenata s dijabetesom tipa 1 i 2. Primarni parametar djelotvornosti za većinu studija bio je glikemijska kontrola, mjerena smanjenjem hemoglobina A1c s početne vrijednosti (HbA1c).
Dijabetes tipa 1
Provedena je 24-tjedna, randomizirana, otvorena studija aktivne kontrole (Studija A) u bolesnika s dijabetesom tipa 1 da bi se procijenila sigurnost i učinkovitost Exubera je primijenjena prije obroka tri puta dnevno (TID) s jednom noćnom injekcijom Humulin® U Ultralente® (humani inzulin s produženom suspenzijom cinka) (n = 136). Uporedni tretman bio je potkožni redoviti humani inzulin primijenjen dva puta dnevno (BID) (prije doručka i prije večere) s BID injekcijom NPH humanog inzulina (suspenzija ljudskog inzulina izofana) (n = 132). U ovom istraživanju prosječna dob bila je 38,2 godine (raspon: 20-64), a 52% ispitanika bili su muškarci.
Druga, randomizirana, otvorena studija aktivne kontrole u trajanju od 24 tjedna, provedena u bolesnika s dijabetesom tipa 1 provedena je radi procjene sigurnost i djelotvornost lijeka Exubera (n = 103) u usporedbi s potkožnim redovitim ljudskim inzulinom (n = 103) kada se primjenjuje TID prije obroka. U obje ruke za liječenje, NPH ljudskom inzulinu primjenjivan je BID (ujutro i prije spavanja) kao bazni inzulin. U ovom istraživanju prosječna dob bila je 38,4 godine (raspon: 19-65), a 54% ispitanika bili su muškarci.
U svakoj su studiji smanjenje HbA1c i stope hipoglikemije bili usporedivi za dvije skupine liječenja. U bolesnika liječenih egzuberima došlo je do većeg smanjenja glukoze u plazmi nakon posta u odnosu na bolesnike iz usporedne skupine. Postotak pacijenata koji dosežu razinu HbA1c <8% (po akciji liječenja Američkog udruženja za dijabetes) Razina u vrijeme provođenja studije) i razina HbA1c <7% bila je usporediva između dvije skupine liječenja. Rezultati za studije A i B prikazani su u tablici 2.
Tablica 2: Rezultati dva 24-tjedna, aktivna kontrola, otvorena ispitivanja u bolesnika s dijabetesom tipa 1 (studije A i B)
| Studija A | Studija B | |||
|---|---|---|---|---|
| Exubera (TID) + UL (QD) | SC R (BID) + NPH (BID) | Exubera (TID) + NPH (BID) | SC R (TID) + NPH (BID) | |
| Veličina uzorka | 136 | 132 | 103 | 103 |
| UL = Humulin® U Ultralente®; SC R = potkožni regularni humani inzulin | ||||
| ||||
| HbA1c (%) | ||||
| Osnovna srednja vrijednost | 7.9 | 8.0 | 7.8 | 7.8 |
| Adj. znači srednja promjena od početne | -0.2 | -0.4 | -0.3 | -0.2 |
| Exubera minus SC R* | 0.14 | -0.11 | ||
| 95% CI za razliku u liječenju | (-0.03, 0.32) | (-0.30, 0.08) | ||
| Plazma glukoza nakon posta (mg / dL) | ||||
| Osnovna srednja vrijednost | 191 | 198 | 178 | 191 |
| Adj. znači srednja promjena od početne | -32 | -6 | -23 | 13 |
| Exubera minus SC R | -27 | -35 | ||
| 95% CI za razliku u liječenju | (-47, -6) | (-58, -13) | ||
| 2-satna koncentracija glukoze u post-prandialu (mg / dL) | ||||
| Osnovna srednja vrijednost | 283 | 305 | 273 | 293 |
| Adj. znači srednja promjena od početne | -21 | 14 | -1 | -3 |
| Exubera minus SC R | -35 | 2 | ||
| 95% CI za razliku u liječenju | (-61, -8) | (-29, 32) | ||
| Pacijenti s završetkom ispitivanja HbA1c < 8%†| 64.0% | 68.2% | 74.8% | 66.0% |
| Pacijenti s završetkom ispitivanja HbA1c < 7% | 16.9% | 19.7% | 28.2% | 30.1% |
| Tjelesna težina | ||||
| Osnovna srednja vrijednost (kg) | 77.4 | 76.4 | 76.0 | 76.9 |
| Adj. srednja promjena od početne (kg) | 0.4 | 1.1 | 0.4 | 0.6 |
| Exubera minus SC R | -0.72 | -0.24 | ||
| 95% CI za razliku u liječenju | (-1.48, 0.04) | (-1.07, 0.59) | ||
| Kraj studije dnevna doza inzulina | ||||
| Inzulin kratkog djelovanja | 13,4 mgc | 18.3 IU | 10,9 mgc | 25,7 IU |
| Inzulin dugog djelovanja | 26,4 IU | 37.1 IU | 31,5 IU | 31,9 IU |
Dijabetes tipa 2
Monoterapija u bolesnika koja nije optimalno kontrolirana dijetom i vježbanjem
Izvršena je 12-tjedna, randomizirana, otvorena studija aktivne kontrole (Studija C) u bolesnika s dijabetesom tipa 2 ne optimalno kontrolirane dijetom i vježbanjem, ocjenjujući sigurnost i djelotvornost prije obroka TID Exubera (n = 75) u usporedbi s sredstvo osjetljivo na inzulin. U ovom istraživanju prosječna dob bila je 53,7 godina (raspon: 28-80), 55% ispitanika bili su muškarci, a srednji indeks tjelesne mase 32,3 kg / m2.
U 12 tjedana HbA1c razina u bolesnika liječenih lijekom Exubera smanjila se za 2,2% (SD = 1,0) od početne vrijednosti 9,5% (SD = 1,1). Udio bolesnika liječenih lijekom Exubera koji su dostigli na kraju studije HbA1c razina <8% porasla je na 82,7%. Udio bolesnika liječenih lijekom Exubera koji su dostigli na kraju studije HbA1c razina
Monoterapija i dodatna terapija u bolesnika prethodno liječenih oralnom terapijom
Provedena je 12-tjedna randomizirana, otvorena studija aktivne kontrole (studija D) u bolesnika s tipom Dijabetes koji su trenutno bili na liječenju, ali slabo kontrolirani, s dva oralna sredstva (OA). Osnovne OA uključuju inzulinski sekretagog i metformin ili tiazolidindion. Bolesnici su nasumično raspoređeni u jednu od tri ruke: samostalno nastavljaju OA terapiju (n = 96), prelaze na monoterapija TID Exubera prije jela (n = 102) ili dodavanje TID Exubere prije obroka kontinuiranoj terapiji OA (n = 100). U ovom istraživanju prosječna dob bila je 57,4 godine (raspon: 33-80), 66% ispitanika bilo je muškaraca, a srednji indeks tjelesne mase 30 kg / m2.
Monoterapija Exubera i Exubera u kombinaciji s OA terapijom bile su superiorne u odnosu na OA terapiju u smanjenju HbA1c razine od početne vrijednosti. Stope hipoglikemije za dvije skupine liječenja Exuberom bile su neznatno veće nego u samoj skupini s OA terapijom. U usporedbi samo s OA terapijom, postotak pacijenata koji dosežu HbA1c razina <8% (po akcijskoj razini liječenja Američkog udruženja za dijabetes u vrijeme provođenja studije) i HbA1c razina <7% bila je veća za bolesnike liječene monoterapijom Exubera i Exubera u kombinaciji s OA terapijom. Pacijenti u obje skupine za liječenje lijekom Exubera imali su veća smanjenja glukoze u plazmi naglo u odnosu na bolesnike liječene samo OA terapijom. Rezultati za Studiju D prikazani su u tablici 3.
Tablica 3: Rezultati 12-tjednog, aktivnog nadzora, otvorenog ispitivanja u bolesnika s dijabetesom tipa 2 koji nisu optimalno kontrolirani dvostrukom oralnom terapijom (studija D)
| Studija D | Exubera monoterapija | OAS* | Exubera + OA |
|---|---|---|---|
| Veličina uzorka | 102 | 96 | 100 |
| |||
| HbA1c (%) | |||
| Osnovna srednja vrijednost | 9.3 | 9.3 | 9.2 |
| Adj. znači srednja promjena od početne | -1.4 | -0.2 | -1.9 |
| Exubera grupa minus OA†| -1.18†,c, § | -1.67†, ¶, § | |
| 95% CI za razliku u liječenju | (-1.41, -0.95) | (-1.90, -1.44) | |
| Plazma glukoza nakon posta (mg / dL) | |||
| Osnovna srednja vrijednost | 203 | 203 | 195 |
| Adj. znači srednja promjena od početne | -23 | 1 | -53 |
| Exubera grupa minus OA | -24c | -53 ¶ | |
| 95% CI za razliku u liječenju | (-36, -11) | (-66, -41) | |
| Pacijenti s završetkom ispitivanja HbA1c < 8%# | 55.9% | 18.8% | 86.0% |
| Pacijenti s završetkom ispitivanja HbA1c < 7% | 16.7% | 1.0% | 32.0% |
| Tjelesna težina | |||
| Osnovna srednja vrijednost (kg) | 89.5 | 88.0 | 88.6 |
| Adj. srednja promjena od početne (kg) | 2.8 | 0.0 | 2.7 |
| Exubera grupa minus OA | 2.80c | 2.75 ¶ | |
| 95% CI za razliku u liječenju | (1.94, 3.65) | (1.89, 3.61) |
Provedena je 24-tjedna, randomizirana, otvorena studija aktivne kontrole (studija E) u bolesnika s dijabetesom tipa 2, koji trenutno primaju sulfonilureju. Ova je studija dizajnirana za procjenu sigurnosti i učinkovitosti dodavanja Exubere prije obroka terapija sulfonilurejom (n = 214) u usporedbi s dodavanjem metformina prije obroka kontinuiranoj terapiji sulfonilurejom (n = 196). Ispitanici su stratificirani prema HbA1c u 1. tjednu. Definirane su dvije slojeve: nizak sloj HbA1c (HbA)1c ‰ ¥ 8% do ¤ 9,5%) i visoki HbA1c stratum (HbA)1c > 9,5 do ‰ ¤12%).
Exubera je u kombinaciji sa sulfonilurejom bila bolja od metformina i sulfonilureje u smanjenju vrijednosti HbA1c od početnih u skupini sa visokim slojem. Exubera je u kombinaciji sa sulfonilureom bila usporediva s metforminom u kombinaciji sa sulfonilurejom u smanjenju vrijednosti HbA1c od početnih u skupini sa niskim slojem. Stopa hipoglikemije bila je veća nakon dodavanja Exubera sulfonilureji nego nakon dodatka metformina u sulfonilureju. Postotak bolesnika koji su dosegli ciljane vrijednosti HbA1c od 8% i 7% bio je usporediv između skupina liječenja u oba sloja, kao i smanjenje glukoze u plazmi na testu (vidjeti Tablica 4).
Sljedeća 24-tjedna, randomizirana, otvorena studija aktivne kontrole (Studija F) provedena je kod bolesnika s dijabetesom tipa 2, koji trenutno primaju metforminsku terapiju. Ova je studija dizajnirana za procjenu sigurnosti i učinkovitosti dodavanja Exubere prije obroka terapija metforminom (n = 234) u usporedbi s dodatkom glibenklamida prije obroka kontinuiranom liječenju metforminom (n = 222). Subjekti u ovoj studiji također su stratificirani u jedan od dva sloja kako je definirano u Studiji E.
Exubera je u kombinaciji s metforminom bila bolja od glibenklamida i metformina u smanjenju HbA1c vrijednosti iz početne vrijednosti i postizanje ciljanog HbA1c vrijednosti u skupini visokog sloja. Exubera je u kombinaciji s metforminom bila usporediva s glibenklamidom u kombinaciji s metforminom u smanjenju HbA1c vrijednosti iz početne vrijednosti i postizanje ciljanog HbA1c vrijednosti u skupini s niskim stratumom. Brzina hipoglikemije bila je neznatno viša nakon dodavanja Exubere metmetinu nego nakon dodatka glibenklamida u metformin. Smanjenje glukoze u plazmi nakon posta bilo je usporedivo između skupina liječenja (vidi Tablica 4).
Tablica 4: Rezultati dvaju 24-tjednih, aktivnih kontrola, otvorenih ispitivanja u bolesnika s dijabetesom tipa 2, prije terapije oralnim agensima (studije E i F)
| Studija E | Studija F | |||||||
|---|---|---|---|---|---|---|---|---|
| Exubera + SU* | Met*+ SU* | Exubera + SU* | Met*+ SU* | Exubera + Met* | Gli* + Met* | Exubera + Met* | Gli* + Met* | |
| Visoka slojeva†| Nizak sloj†| Visoka slojeva†| Nizak sloj†| |||||
| Veličina uzorka | 113 | 103 | 101 | 93 | 109 | 103 | 125 | 119 |
| ||||||||
| HbA1c (%) | ||||||||
| Osnovna srednja vrijednost | 10.5 | 10.6 | 8.8 | 8.8 | 10.4 | 10.6 | 8.6 | 8.7 |
| Adj. znači srednja promjena od početne | -2.2 | -1.8 | -1.9 | -1.9 | -2.2 | -1.9 | -1.8 | -1.9 |
| Exubera minus OAc | -0.38c, § | -0.07 | -0.37c, ¶ | 0.04 | ||||
| 95% CI za razliku u liječenju | (-0.63, -0.14) | (-0.33, 0.19) | (-0.62, -0.12) | (-0.19, 0.27) | ||||
| Plazma glukoza nakon posta (mg / dL) | ||||||||
| Osnovna srednja vrijednost | 241 | 237 | 197 | 198 | 223 | 243 | 187 | 196 |
| Srednja promjena od početne vrijednosti | -46 | -47 | -48 | -52 | -42 | -40 | -46 | -49 |
| Exubera minus OA | 1 | 4 | -2 | 4 | ||||
| 95% CI za razliku u liječenju | (-11, 12) | (-8, 16) | (-14, 10) | (-7, 15) | ||||
| Ispitanici sa završetkom ispitivanja HbA1c < 8%# | 48.7% | 44.7% | 81.2% | 73.1% | 72.5% | 56.3% | 80.8% | 86.6% |
| Ispitanici sa završetkom ispitivanja HbA1c < 7% | 20.4% | 14.6% | 30.7% | 32.3% | 33.9% | 17.5% | 40.0% | 42.9% |
| Tjelesna težina | ||||||||
| Osnovna srednja vrijednost (kg) | 80.8 | 79.5 | 79.9 | 81.9 | 88.3 | 87.8 | 90.3 | 88.2 |
| Adj. srednja promjena od početne (kg) | 3.6 | -0.0 | 2.4 | -0.3 | 2.8 | 2.5 | 2.0 | 1.6 |
| Exubera minus OA | 3.60 | 2.67 | 0.26 | 0.38 | ||||
| 95% CI za razliku u liječenju | (2.81, 4.39) | (1.84, 3.51) | (-0.70, 1.21) | (-0.52, 1.27) |
Primjena kod pacijenata prethodno liječenih subkutanim inzulinom
Provedena je 24-tjedna, randomizirana, otvorena studija aktivne kontrole (Studija G) u bolesnika liječenih inzulinom tipa 2 dijabetesa za procjenu sigurnosti i djelotvornosti lijeka Exubera koji je primijenjen TID prije obroka uz jednu noćnu injekciju Humulin® U Ultralente® (n = 146) u usporedbi s potkožnim redovitim ljudskim inzulinom koji se daje BID (prije doručka i prije večere) s BID injekcijom NPH humanog inzulina (n = 149). U ovom istraživanju prosječna dob bila je 57,5 godina (raspon: 23-80), 66% ispitanika bili su muškarci, a srednji indeks tjelesne mase 30,3 kg / m2.
Smanjenja od osnovne vrijednosti u HbA1c, postotak pacijenata koji dosežu HbA1c razina <8% (po akcijskoj razini liječenja Američkog udruženja za dijabetes u vrijeme provođenja studije) i HbA1c razina <7%, kao i stope hipoglikemije, bile su slične između skupina liječenja. U bolesnika liječenih egzuberima došlo je do većeg smanjenja glukoze u plazmi nakon posta u odnosu na bolesnike iz usporedne skupine. Rezultati za Studiju G prikazani su u tablici 5.
Tablica 5: Rezultati 24-tjednog, aktivnog nadzora, otvorenog ispitivanja u bolesnika s dijabetesom tipa 2, prethodno liječenih subkutanim inzulinom (studija G)
| Studija G | Exubera (TID) + UL (QD) | SC R (BID) + NPH (BID) |
|---|---|---|
| Veličina uzorka | 146 | 149 |
| UL = Humulin® U Ultralente®; SC R = potkožni regularni humani inzulin | ||
| ||
| HbA1c (%) | ||
| Osnovna srednja vrijednost | 8.1 | 8.2 |
| Adj. znači srednja promjena od početne | -0.7 | -0.6 |
| Exubera minus SC R* | -0.07 | |
| 95% CI za razliku u liječenju | (-0.31, 0.17) | |
| Plazma glukoza nakon posta (mg / dL) | ||
| Osnovna srednja vrijednost | 152 | 159 |
| Adj. znači srednja promjena od početne | -22 | -6 |
| Exubera minus SC R | -16.36 | |
| 95% CI za razliku u liječenju | (-27.09, -5.36) | |
| Pacijenti s završetkom ispitivanja HbA1c < 8%†| 76.0% | 69.1% |
| Pacijenti s završetkom ispitivanja HbA1c < 7% | 45.2% | 32.2% |
| Tjelesna težina | ||
| Osnovna srednja vrijednost (kg) | 90.6 | 89.0 |
| Adj. srednja promjena od početne (kg) | 0.1 | 1.3 |
| Exubera minus SC R | -1.28 | |
| 95% CI za razliku u liječenju | (-1.96, -0.60) | |
| Kraj studije dnevna doza inzulina | ||
| Inzulin kratkog djelovanja | 16,6 mgc | 25,5 IU |
| Inzulin dugog djelovanja | 37,9 IU | 52,3 IU |
vrh
Indikacije i upotreba
Exubera je indicirana za liječenje odraslih bolesnika sa šećernom bolešću radi kontrole hiperglikemije. Exubera ima učinak sličan analogima inzulina brzog djelovanja i ima trajanje aktivnosti snižavanja glukoze usporedivo s supkutano primijenjenim ljudskim inzulinom. U bolesnika s dijabetesom tipa 1, Exubera treba koristiti u režimima koji uključuju inzulin dužeg djelovanja. U bolesnika s dijabetesom tipa 2, Exubera se može koristiti kao monoterapija ili u kombinaciji s oralnim agensima ili duljim djelovanjem inzulina.
vrh
kontraindikacije
Exubera je kontraindicirana u bolesnika preosjetljivih na Exubera ili neku od njegovih pomoćnih tvari.
Exubera je kontraindicirana u bolesnika koji puše ili koji su prestali pušiti manje od 6 mjeseci prije početka terapije Exuberom. Ako pacijent započne ili nastavi pušiti, lijek Exubera mora se odmah prekinuti zbog povećanog rizika od hipoglikemije i mora se koristiti alternativno liječenje (vidjeti KLINIČKA FARMAKOLOGIJA, Posebne populacije, pušenje). Sigurnost i djelotvornost lijeka Exubera u bolesnika koji puše nisu utvrđeni.
Exubera je kontraindicirana u bolesnika s nestabilnom ili slabo kontroliranom bolešću pluća, zbog velikih varijacija u funkciji pluća što bi moglo utjecati na apsorpciju Exubere i povećati rizik od hipoglikemije ili hiperglikemija.
vrh
Upozorenja
Exubera se od uobičajenog ljudskog inzulina razlikuje po brzom početku djelovanja. Kada se koristi kao inzulin za vrijeme obroka, dozu Exubera treba dati u roku od 10 minuta prije obroka.
Hipoglikemija je najčešće prijavljeni štetni događaj inzulinske terapije, uključujući Exubera. Vremena hipoglikemije mogu se razlikovati kod različitih formulacija inzulina.
Pacijenti s dijabetesom tipa 1 također zahtijevaju duže djelovanje inzulina za održavanje odgovarajuće kontrole glukoze.
Svaku promjenu inzulina treba obaviti oprezno i samo pod liječničkim nadzorom. Promjene u jakosti inzulina, proizvođaču, vrsti (npr. Redoviti, NPH, analozi) ili vrstama (životinja, čovjek) mogu rezultirati potrebom za promjenom doziranja. Moguće je podesiti suvremeni oralni antidijabetički tretman.
Praćenje glukoze preporučuje se svim pacijentima koji imaju dijabetes.
Zbog učinka Exubere na plućnu funkciju, svi bolesnici trebali bi procijeniti plućnu funkciju prije započinjanja terapije lijekom Exubera (vidjeti MJERE OPREZA: Plućna funkcija).
Primjena lijeka Exubera u bolesnika s osnovnom plućnom bolešću, poput astme ili KOPB-a, ne preporučuje se, jer sigurnost i djelotvornost lijeka Exubera u ovoj populaciji nije utvrđena (vidjeti MJERE OPREZA: Temeljna bolest pluća).
U kliničkim ispitivanjima Exubere, zabilježeno je 6 novo dijagnosticiranih slučajeva primarnih malignih bolesti pluća kod pacijenata liječenih Exuberom, te 1 novo dijagnosticirani slučaj među bolesnicima koji su liječeni komparativno. Objavljeno je i 1 izvješće o stavljanju na tržište primarnog malignog oboljenja pluća kod pacijenta liječenog lijekom Exubera. U kontroliranim kliničkim ispitivanjima Exubere incidencija novog primarnog karcinoma pluća tijekom 100 izloženih lijekova tijekom godina ispitivanja bila je 0,13 (5 slučajeva više od 3900 pacijentskih godina) za bolesnike liječene lijekom Exubera i 0,02 (1 slučaj više od 4100 pacijenata godina) za bolesnike liječene komparacijom. Bilo je premalo slučajeva da bi se utvrdilo je li pojava tih događaja povezana s Exuberom. Svi pacijenti kojima je dijagnosticiran rak pluća imali su prethodnu povijest pušenja cigareta.
vrh
Mjere opreza
Općenito
Kao i kod svih inzulinskih pripravaka, vremenski tijek djelovanja Exubera može se razlikovati kod različitih pojedinaca ili u različitom vremenu kod iste osobe. Prilagodba doziranja bilo kojeg inzulina može biti potrebna ako pacijenti promijene fizičku aktivnost ili svoj uobičajeni plan obroka. Potrebe za inzulinom mogu se mijenjati tijekom interkventnih stanja kao što su bolest, emocionalni poremećaji ili stres.
Hipoglikemija
Kao i kod svih inzulinskih pripravaka, hipoglikemijske reakcije mogu biti povezane s primjenom Exubera. Brze promjene koncentracije glukoze u serumu mogu izazvati simptome slične hipoglikemiji kod osoba s dijabetesom, bez obzira na vrijednost glukoze. Simptomi ranog upozoravanja hipoglikemije mogu biti različiti ili manje izraženi pod određenim uvjetima, kao što je dugo trajanje dijabetesa, bolesti dijabetičkih živaca, uporaba lijekova poput beta blokatora ili pojačana kontrola dijabetesa (vidjeti MJERE OPREZA: Interakcije s lijekovima). Takve situacije mogu rezultirati ozbiljnom hipoglikemijom (i, moguće, gubitkom svijesti) prije nego što pacijenti postanu svjesni hipoglikemije.
Oštećenje bubrega
Ispitivanja nisu provedena u bolesnika s oštećenjem bubrega. Kao i kod ostalih inzulinskih pripravaka, doza potrebna za Exubera može se smanjiti u bolesnika s oštećenjem bubrega (vidjeti KLINIČKA FARMAKOLOGIJA, Posebne populacije).
Oštećenje jetre
Ispitivanja nisu provedena na bolesnicima s oštećenjem jetre. Kao i kod drugih inzulinskih pripravaka, doza za Exuberu može se smanjiti u bolesnika s oštećenjem jetre (vidjeti KLINIČKA FARMAKOLOGIJA, Posebne populacije).
Alergija
Sistemska alergija
U kliničkim ispitivanjima, ukupna učestalost alergijskih reakcija u bolesnika liječenih Exuberom bila je slična onoj u bolesnika koji su koristili subkutane režime s redovitim ljudskim inzulinom.
Kao i kod drugih inzulinskih pripravaka, može se pojaviti rijetka, ali potencijalno ozbiljna generalizirana alergija na inzulin, što može uzrokovati osip (uključujući pruritus) po cijelom tijelu, kratkoća daha, piskanje u vodi, smanjenje krvnog tlaka, ubrzani puls ili znojenje. Teški slučajevi generalizirane alergije, uključujući anafilaktičke reakcije, mogu biti opasni po život. Ako se takve reakcije pojave od Exubere, Exubera treba prekinuti i razmotriti alternativne terapije.
Proizvodnja antitijela
Antitijela za inzulin mogu se razviti tijekom liječenja svim inzulinskim pripravcima, uključujući Exubera. U kliničkim studijama Exubere gdje je komparator bio supkutani inzulin, povećava se razina inzulinskih antitijela (što se odražava analizama aktivnost vezanja na inzulin) bile su značajno veće za bolesnike koji su primali Exubera nego za bolesnike koji su primali potkožni inzulin samo. Nisu utvrđene kliničke posljedice ovih antitijela tijekom vremenskog razdoblja kliničkih studija Exubere; međutim, dugoročni klinički značaj ovog povećanja stvaranja antitijela nije poznat.
respiratorni
Plućna funkcija
U kliničkim ispitivanjima u trajanju do dvije godine, pacijenti liječeni Exuberom pokazali su veći pad plućne funkcije, posebno prisilni volumen ekspiratora u jednoj sekundi (FEV1) i kapacitet difuzije ugljičnog monoksida (DLCO), nego tretirano komparativno pacijenata. Uobičajena je razlika u skupini liječenja u plućnoj funkciji koja favorizira komparativnu skupinu prvih nekoliko tjedana liječenja Exuberom, a nije se mijenjalo tijekom dvogodišnjeg razdoblja liječenja (Vidjeti NEPOVOLJNI REAKCIJE: Plućna funkcija).
Tijekom kontroliranih kliničkih ispitivanja, pojedinačni su pacijenti zabilježili značajan pad plućne funkcije u obje skupine liječenja. Pad sa početnog FEV1 od ¥ ¥ 20% kod posljednjeg promatranja dogodio se kod 1,5% liječenih Exuberom i 1,3% bolesnika koji su primali komparaciju. Pad od osnovne DLCO od ‰ ¥ 20% u posljednjem opažanju pojavilo se u 5,1% liječenih Exuberom i 3,6% bolesnika koji su primali komparaciju.
Zbog učinka Exubere na plućnu funkciju, svi bolesnici trebali bi provesti spirometriju (FEV1) prije započinjanja terapije lijekom Exubera. Procjena DL-aCO treba razmotriti. Učinkovitost i sigurnost lijeka Exubera u bolesnika s početnom FEV-om1 ili DLCO <70% predviđenih nije utvrđeno, pa se uporaba Exubere u ovoj populaciji ne preporučuje.
Procjena plućne funkcije (npr. Spirometrija) preporučuje se nakon prvih 6 mjeseci terapije, a nakon toga godišnje, čak i ako nema plućnih simptoma. U bolesnika koji imaju pad od ‰ ¥% 20% u odnosu na početnu vrijednost, testovi plućne funkcije trebaju se ponoviti. Ako je potvrđen pad od 20% od početnog FEV1, Exubera treba prekinuti. Prisutnost plućnih simptoma i manji pad plućne funkcije mogu zahtijevati češće praćenje plućne funkcije i razmatranje prekida lijeka Exubera.
Temeljna bolest pluća
Primjena Exubere u bolesnika s osnovnom plućnom bolešću, poput astme ili KOPB-a, ne preporučuje se jer učinkovitost i sigurnost Exubere u ovoj populaciji nisu utvrđene.
bronhospazam
Bronhospazam je rijetko prijavljen u bolesnika koji uzimaju Exubera. Pacijenti koji su imali takvu reakciju trebali bi prekinuti lijek Exubera i odmah potražiti liječničku procjenu. Ponovna primjena lijeka Exubera zahtijeva pažljivu procjenu rizika i treba ga izvoditi samo pod strogim medicinskim nadzorom s odgovarajućim kliničkim ustanovama.
Interkurentna respiratorna bolest
Tijekom primjene kliničkih ispitivanja, Exubera se primjenjuje na pacijente s interkurentnim respiratornim bolestima (npr. Bronhitisom, infekcijama gornjih dišnih puteva, rinitisom). U bolesnika koji su imali ova stanja, 3-4% privremeno prekinulo terapiju lijekom Exubera. Nije zabilježen povećan rizik od hipoglikemije ili pogoršane kontrole glikemije u bolesnika liječenih Exuberom u usporedbi s pacijentima liječenima potkožnim inzulinom. Tijekom intercurrentnih bolesti dišnog sustava može biti potrebno pažljivo praćenje koncentracija glukoze u krvi i prilagođavanje doze.
Informacije za pacijente
Pacijente treba poučavati o postupcima samoupravljanja, uključujući praćenje glukoze; pravilna tehnika inhalacije Exubera; te hipoglikemija i liječenje hiperglikemije. Pacijenti moraju biti upućeni na postupanje u posebnim situacijama kao što su interkventna stanja (bolest, stres ili emocionalna stanja) poremećaji), neadekvatna ili preskočena doza inzulina, nenamjerna primjena povećane doze inzulina, neadekvatni unos hrane ili preskočeni obroci.
Bolesnike treba obavijestiti da je u kliničkim ispitivanjima liječenje lijekom Exubera povezano s malim, neprogresivnim srednjim padima plućne funkcije u odnosu na usporedne tretmane. Zbog učinka lijeka Exubera na plućnu funkciju, preporuča se testiranje plućne funkcije prije započinjanja liječenja lijekom Exubera. Nakon započinjanja terapije preporučuju se periodični testovi plućne funkcije (vidjeti MJERE OPREZA Respiratorna, plućna funkcija).
Pacijenti bi trebali obavijestiti svog liječnika ako imaju povijest plućnih bolesti, jer se primjena Exubera ne preporučuje u bolesnika s osnovnom plućnom bolešću (npr. astma ili KOPB), a kontraindiciran je bolesnicima s slabo kontroliranim plućima bolest.
Ženama s dijabetesom treba savjetovati da obavijeste svog liječnika ako su trudne ili razmišljaju o trudnoći.
vrh
Interakcije s lijekovima
Brojne tvari utječu na metabolizam glukoze pa mogu zahtijevati prilagođavanje doze inzulina i posebno pažljivo praćenje.
Slijede primjeri tvari koje mogu smanjiti učinak inzulina na snižavanje glukoze u krvi što može rezultirati hiperglikemijom: kortikosteroidi, danazol, diazoksid, diuretici, simpatomimetičari (npr. epinefrin, albuterol, terbutalin), derivati glukagona, izoniazid, fenotiazin, somatropin, hormoni štitnjače, estrogeni, progestogeni (npr., u oralnim kontraceptivima), inhibitori proteaze i atipični antipsihotici (npr. olanzapin i klozapin).
Slijede primjeri tvari koje mogu pojačati učinak inzulina na snižavanje glukoze u krvi i osjetljivost na hipoglikemiju: oralno antidijabetički proizvodi, ACE inhibitori, disopiramid, fibrati, fluoksetin, MAO inhibitori, pentoksifilin, propoksifen, salicilati i sulfonamid antibiotici.
Beta blokatori, klonidin, litijeve soli i alkohol mogu ili povećati ili smanjiti učinak inzulina na snižavanje glukoze u krvi. Pentamidin može izazvati hipoglikemiju, koja ponekad može biti praćena hiperglikemijom.
Osim toga, pod utjecajem simpatolitičkih lijekova poput beta blokatora, klonidina, gvanetidina i rezerpina, znakovi i simptomi hipoglikemije mogu se smanjiti ili izostati.
Bronhodilatatori i drugi inhalacijski proizvodi mogu promijeniti apsorpciju ljudskog inzulina koji se inhalira (vidjeti KLINIČKA FARMAKOLOGIJA, Posebne populacije). Preporučuje se dosljedno vrijeme doziranja bronhodilatatora u odnosu na primjenu Exubera, pažljivo praćenje koncentracija glukoze u krvi i titracija doze prema potrebi.
Kancerogeneza, mutageneza, oštećenje plodnosti
Dvogodišnja ispitivanja kancerogenosti na životinjama nisu provedena. Incesin inzulin nije bio mutagen u Ames bakterijskom reverznom mutacijskom testu u prisutnosti i odsutnosti metaboličke aktivacije.
U štakora Sprague-Dawley, provedeno je 6-mjesečno ispitivanje toksičnosti za ponavljanje doze s prahom za inhalaciju inzulina u dozama do 5,8 mg / kg / dan (u usporedbi s kliničkim početna doza od 0,15 mg / kg / dan, visoka doza za štakor bila je 39 puta ili 8,3 puta veća od kliničke doze, na temelju usporedbe površine mg / kg ili mg / m2 tjelesne površine). Kod majmuna Cynomolgus provedena je 6-mjesečna studija toksičnosti s ponavljanjem doze s inhaliranim inzulinom u dozama do 0,64 mg / kg / dan. U usporedbi s kliničkom početnom dozom od 0,15 mg / kg / dan, velika doza majmuna bila je 4,3 puta ili 1,4 puta veća od kliničke doze, na temelju usporedbe površine mg / kg ili mg / m2 tjelesne površine. To su bile maksimalno tolerirane doze temeljene na hipoglikemiji.
U usporedbi s kontrolnim životinjama, nije bilo neželjenih učinaka povezanih s liječenjem bilo koje vrste na plućnu funkciju, grubu ili mikroskopsku morfologiju dišnih putova ili bronhijalnih limfnih čvorova. Slično tomu, nijedna vrsta nije utjecala na indekse stanične proliferacije u alveolarnim ili bronhiolarnim područjima pluća.
Budući da je rekombinantni humani inzulin identičan endogenom hormonu, ispitivanja reproduktivne / plodnosti na životinjama nisu provedena.
Trudnoća
Teratogeni učinci
Trudnoća Kategorija C
Studije reprodukcije životinja nisu provedene s Exuberom. Također nije poznato može li Exubera nanijeti plodnu štetu prilikom primjene trudnica ili može li Exubera utjecati na reproduktivnu sposobnost. Exubera se daje trudnici samo ako je to očigledno potrebno.
Negovateljice
Mnogi lijekovi, uključujući ljudski inzulin, izlučuju se u majčino mlijeko. Iz tog razloga, oprez treba biti oprezan kada se Exubera daje nekoj ženi. Bolesnicima s dijabetesom koji doje mogu biti potrebne prilagodbe doze Exubera, plana obroka ili oboje.
Dječja upotreba
Dugoročna sigurnost i učinkovitost Exubere u pedijatrijskih bolesnika nisu utvrđene (vidjeti KLINIČKA FARMAKOLOGIJA, Posebne populacije).
Gerijatrijska upotreba
U kontroliranim kliničkim ispitivanjima Phase 2/3 (n = 1975), Exubera je primjenjivan na 266 bolesnika u dobi od 65 godina i 30 bolesnika u dobi od 75 godina. Većina tih bolesnika imala je dijabetes tipa 2. Promjena HbA1C a stopa hipoglikemije nije se razlikovala prema dobi.
vrh
Nuspojave
Sigurnost samog Exubere, ili u kombinaciji s potkožnim inzulinom ili oralnim agensima, bila je procijenjena na otprilike 2500 odraslih pacijenata s dijabetesom tipa 1 ili tipa 2 koji su bili izloženi Exubera. Otprilike 2000 bolesnika bilo je izloženo Exuberi duže od 6 mjeseci, a više od 800 bolesnika bilo je izloženo više od 2 godine.
Ne-respiratorni neželjeni događaji
Ne-respiratorni neželjeni događaji prijavljeni u ¥% 1% bolesnika liječenih Exuberom u kontroliranim kliničkim studijama faze 2/3, bez obzira na uzročno-posljedične veze, uključuju (ali nisu ograničeni na) sljedeće:
Metabolički i prehrambeni: hipoglikemija (vidjeti UPOZORENJA i MJERE OPREZA)
Tijelo u cjelini: bol u prsima
Probava: suha usta
Specijalna osjetila: otitis media (tip 1 dječji dijabetičari)
Hipoglikemija
Stope i učestalost hipoglikemije bili su usporedivi između Exubere i subkutanog redovitog ljudskog inzulina u bolesnika s dijabetesom tipa 1 i 2. U bolesnika tipa 2 koji nisu bili adekvatno kontrolirani jedinstvenom terapijom oralnim agensima, dodavanje Exubera je bila povezana s većom stopom hipoglikemije nego što je bio dodavanje druge oralne agent.
Bol u prsima
Za niz različitih simptoma u prsima prijavljeni su kao nuspojave i grupirani su pod nespecifični pojam boli u prsima. Ovi se događaji pojavili u 4,7% bolesnika liječenih Exuberom i 3,2% bolesnika u usporednim skupinama. Većina (> 90%) tih događaja prijavljena je kao blaga ili umjerena. Dva pacijenta iz skupine Exubera i jedan iz usporedne skupine prekinuli su liječenje zbog bolova u prsima. Učestalost nuspojava od kauzaliteta povezanih s koronarnom arterijskom bolešću, kao što su angina pektoris ili infarkt miokarda, bila je usporediva u mjestu Exubera (0,7% angine pectoris; 0,7% infarkta miokarda) i komparatora (1,3% angine pektoris; 0,7% skupina liječenja infarkta miokarda).
Suha usta
Zabilježena su suha usta u 2,4% bolesnika liječenih Exuberom i 0,8% bolesnika u usporednim skupinama. Gotovo svi (> 98%) prijavljenih suhih usta bili su blagi ili umjereni. Nijedan pacijent nije prekinuo liječenje zbog suhoće usta.
Učni događaji u pedijatrijskih dijabetičara
Pedijatrijski dijabetičari tipa 1 u skupinama Exubera imali su češće štetne događaje vezane za uho nego pedijatrijski dijabetičari tipa 1 u skupinama koje su primale samo potkožni inzulin. Ti su događaji uključivali otitis media (Exubera 6,5%; SC 3,4%), bol u uhu (Exubera 3,9%; SC 1,4%) i poremećaj ušiju (Exubera 1,3%; SC 0%).
Respiratorni neželjeni događaji
Tablica 6 prikazuje učestalost respiratornih nuspojava za svaku tretiranu grupu koja je zabilježena u ¥% 1% bilo koje skupine liječenja u kontroliranim kliničkim ispitivanjima faze 2 i 3, bez obzira na uzročnost.
Tablica 6: Respiratorni neželjeni događaji prijavljeni u ¥ ¥% 1% bilo koje skupine liječenja u kontroliranim fazama 2 i 3 kliničkih studija, bez obzira na uzročnost
| Postotak prijavljivanja događaja pacijenata | |||||
|---|---|---|---|---|---|
| Neželjeni događaj | Dijabetes tipa 1 | Dijabetes tipa 2 | |||
| Exubera N = 698 |
SC N = 705 |
Exubera N = 1279 |
SC N = 488 |
OAS N = 644 |
|
| SC = komparator za potkožni inzulin; OA = komparatori oralnih sredstava | |||||
| Infekcija respiratornog trakta | 43.3 | 42.0 | 29.2 | 38.1 | 19.7 |
| Kašalj povećan | 29.5 | 8.8 | 21.9 | 10.2 | 3.7 |
| upala grla | 18.2 | 16.6 | 9.5 | 9.6 | 5.9 |
| rinitis | 14.5 | 10.9 | 8.8 | 10.5 | 3.0 |
| upala sinusa | 10.3 | 7.4 | 5.4 | 10.0 | 2.3 |
| Respiracijski poremećaj | 7.4 | 4.1 | 6.1 | 10.2 | 1.7 |
| dispneja | 4.4 | 0.9 | 3.6 | 2.5 | 1.4 |
| Povećani ispljuvak | 3.9 | 1.3 | 2.8 | 1.0 | 0.5 |
| Bronhitis | 3.2 | 4.1 | 5.4 | 3.9 | 4.0 |
| Astma | 1.3 | 1.3 | 2.0 | 2.3 | 0.5 |
| epistaksa | 1.3 | 0.4 | 1.2 | 0.4 | 0.8 |
| Upala grla | 1.1 | 0.4 | 0.5 | 0.4 | 0.3 |
| Upala pluća | 0.9 | 1.1 | 0.9 | 1.6 | 0.6 |
| Promjena glasa | 0.1 | 0.1 | 1.3 | 0.0 | 0.3 |
Kašalj
U 3 kliničke studije, pacijenti koji su ispunili upitnik za kašalj izvijestili su da se kašalj pojavljuje unutar sekundi do minuta nakon inhalacije Exubera, bila je pretežno blaga težina i bila je rijetko produktivna u priroda. Učestalost ovog kašlja smanjila se s nastavkom primjene lijeka Exubera. U kontroliranim kliničkim studijama 1,2% bolesnika prekinulo je liječenje lijekom Exubera zbog kašlja.
dispneja
Gotovo svi (> 97%) dispneje su prijavljeni kao blagi ili umjereni. Mali broj bolesnika liječenih Exuberom (0,4%) prekinuo je liječenje zbog dispneje u usporedbi s 0,1% bolesnika koji su primali komparaciju.
Ostali nepovoljni respiratorni događaji - faringitis, pojačana ispljuvka i epistaksa
Većina tih događaja prijavljena je kao blaga ili umjerena. Mali broj bolesnika liječenih lijekom Exubera prekinuo je liječenje zbog faringitisa (0,2%), a ispljuvak se povećao (0,1%); nijedan pacijent nije prekinuo liječenje zbog epistaksa.
Plućna funkcija
Učinak Exubere na dišni sustav procijenjen je u preko 3800 bolesnika u kontroliranim kliničkim ispitivanjima faze 2 i 3 (u kojima su 1977 liječeni lijekom Exubera). U randomiziranim, otvorenim kliničkim ispitivanjima u trajanju do dvije godine, bolesnici liječeni Exuberom pokazao je veći pad plućne funkcije, posebno prisilni volumen ekspiratora u jednom drugi (FEV1) i kapacitet difuzije ugljičnog monoksida (DLCO), nego pacijenti koji su liječeni u usporedbi. Prosječne razlike u skupini liječenja u FEV-u1 i DLCO, zabilježeni su tijekom prvih nekoliko tjedana liječenja Exuberom, a nisu napredovali tijekom dvogodišnjeg razdoblja liječenja. U jednom završenom kontroliranom kliničkom ispitivanju u bolesnika s dijabetesom tipa 2 nakon dvije godine liječenja Exuberom, pacijenti su pokazali rezoluciju razlike u skupini liječenja u FEV-u1 šest tjedana nakon prekida terapije. Rješavanje učinka Exubere na plućnu funkciju u bolesnika s dijabetesom tipa 1 nije proučeno nakon dugotrajnog liječenja.
Slike 3 do 6 prikazuju srednju vrijednost FEV1 i DLCO promjena u odnosu na početnu vrijednost u odnosu na dva tekuća randomizirana otvorena dvogodišnja ispitivanja na 580 bolesnika s dijabetesom tipa 1 i 620 bolesnika s dijabetesom tipa 2.
Slika 3: Promjena s početne vrijednosti FEV1 (L) u bolesnika s dijabetesom tipa 1 (srednje +/- standardno odstupanje)
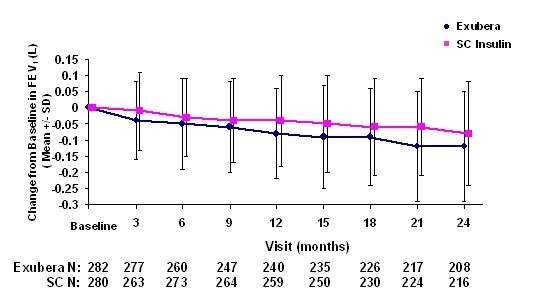
Slika 4: Promjena s početne vrijednosti FEV1 (L) u bolesnika s dijabetesom tipa 2 (srednje +/- standardno odstupanje)

Nakon 2 godine liječenja Exuberom u bolesnika s dijabetesom tipa 1 i 2, razlika između skupina za liječenje prosječna promjena od početne vrijednosti FEV1 iznosila je otprilike 40 ml, što je favoriziralo komparator.
Slika 5: Promjena s bazne DLco (ml / min / mmHg) u bolesnika s dijabetesom tipa 1 (srednje +/- standardno odstupanje)
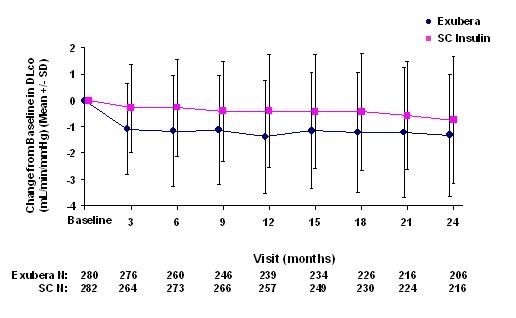
Slika 6: Promjena s bazne DLco (ml / min / mmHg) u bolesnika s dijabetesom tipa 2 (srednje +/- standardno odstupanje)
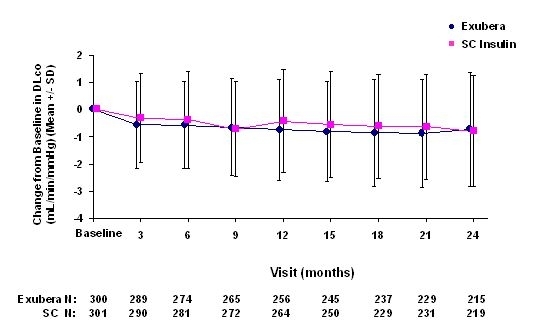
Nakon 2 godine liječenja Exuberom, razlika između skupina liječenja za srednju promjenu od DL početne vrijednostiCO iznosila je oko 0,5mL / min / mmHg (dijabetes tipa 1), favorizirajući usporednik, i približno 0,1mL / min / mmHg (dijabetes tipa 2), favorizirajući Exubera.
Tijekom dvogodišnjeg kliničkog ispitivanja pojedini su pacijenti zabilježili značajan pad plućne funkcije u obje skupine liječenja. Pad od početnog FEV-a1 od ‰ ¥ 20% u posljednjem opažanju pojavilo se kod 1,5% liječenih lijekom Exubera i 1,3% bolesnika koji su primali komparaciju. Pad od osnovne DLCO od ‰ ¥ 20% u posljednjem opažanju pojavilo se u 5,1% liječenih Exuberom i 3,6% bolesnika koji su primali komparaciju.
vrh
predoziranje
Hipoglikemija se može pojaviti kao rezultat viška inzulina u odnosu na unos hrane, potrošnju energije ili oboje.
Blage do umjerene epizode hipoglikemije obično se mogu liječiti oralnom glukozom. Možda će biti potrebne prilagodbe doziranja lijekova, obrasca obroka ili vježbanja.
Teške epizode hipoglikemije s komom, napadajem ili neurološkim oštećenjem mogu se liječiti intramuskularnim / potkožnim glukagonom ili koncentriranom intravenskom glukozom. Trajni unos ugljikohidrata i promatranje mogu biti potrebni jer se hipoglikemija može ponoviti nakon očitog kliničkog oporavka.
vrh
Doziranje i primjena
Exubera, poput brzo djelujućih analoga inzulina, ima brži početak aktivnosti snižavanja glukoze u odnosu na supkutano ubrizgani redovni humani inzulin. Exubera ima trajanje aktivnosti snižavanja glukoze usporedivo s supkutano injiciranim običnim ljudskim inzulinom i duže od inzulina brzog djelovanja. Doze Exubera treba primijeniti neposredno prije obroka (ne više od 10 minuta prije svakog obroka).
U bolesnika s dijabetesom tipa 1, Exubera treba koristiti u režimima koji uključuju inzulin dužeg djelovanja. Za bolesnike s dijabetesom tipa 2, Exubera se može koristiti kao monoterapija ili u kombinaciji s oralnim agensima ili inzulinom dužeg djelovanja.
Zbog učinka lijeka Exubera na plućnu funkciju, svi bi bolesnici trebali imati procjenu plućne funkcije prije započinjanja terapije lijekom Exubera. Preporučuje se periodično nadgledanje plućne funkcije za bolesnike koji se liječe Exuberom (vidjeti MJERE OPREZA, Plućna funkcija).
Exubera je predviđena za primjenu inhalacijom i mora se primijeniti samo pomoću Exubere® Inhalator. Pogledajte u Vodič za lijekove Exubera za opis Exubera® Inhalator i upute za uporabu inhalatora.
Proračun početne doze egzebere prije obroka
Početna doza lijeka Exubera trebala bi biti individualizirana i određena na temelju savjeta liječnika u skladu s potrebama pacijenta. Preporučene početne doze prije obroka temelje se na kliničkim ispitivanjima u kojima je od pacijenata traženo da jedu tri obroka dnevno. Početna doza prije obroka može se izračunati pomoću sljedeće formule: [Tjelesna masa (kg) X 0,05 mg / kg = doza prije obroka (mg)] zaokružena je na najbliži cijeli miligramski broj (npr., 3,7 mg zaokruženo na 3 mg).
Približne smjernice za početne, prije obroka Exubera doze, temeljene na tjelesnoj težini pacijenta, navedene su u tablici 7:
Tablica 7: Približne smjernice za početnu, pre-obročnu dozu egzebere (na temelju tjelesne težine bolesnika)
| Težina pacijenta (u kg) |
Težina pacijenta (u funti) |
Početna doza po obroku | Broj 1 mg blistera po dozi | Broj 3 mg blistera po dozi |
|---|---|---|---|---|
| 30 do 39,9 kg | 66 - 87 lb | 1 mg po obroku | 1 | - |
| 40 do 59,9 kg | 88 - 132 lb | 2 mg po obroku | 2 | - |
| 60 do 79,9 kg | 133 - 176 lb | 3 mg po obroku | - | 1 |
| 80 do 99,9 kg | 177 - 220 lb | 4 mg po obroku | 1 | 1 |
| 100 do 119,9 kg | 221- 264 lb | 5 mg po obroku | 2 | 1 |
| 120 do 139,9 kg | 265 - 308 funti | 6 mg po obroku | - | 2 |
1 mg blistera inzulina inhaliranog Exubere otprilike je ekvivalent 3 IU supkutano injiciranog ljudskog inzulina. 3 mg blistera inzulina inhaliranog Exubera otprilike je ekvivalentno 8 IU supkutano injiciranog ljudskog inzulina. Tablica 8 daje približnu IU dozu redovitog potkožnog humanog inzulina za Exubera inhalacijske doze inzulina od 1 mg do 6 mg.
Tablica 8: Približna ekvivalentna IU doza normalnog humanog supkutanog inzulina za doze inzulina inhilirane egzuberom u rasponu od 1 mg do 6 mg
| Doza (mg) | Približna redovita doza inzulina SC u IU | Broj 1 mg Exubera blistera po dozi | Broj 3 mg Exubera blistera po dozi |
|---|---|---|---|
| 1 mg | 3 | 1 | - |
| 2 mg | 6 | 2 | - |
| 3 mg | 8 | - | 1 |
| 4 mg | 11 | 1 | 1 |
| 5 mg | 14 | 2 | 1 |
| 6 mg | 16 | - | 2 |
Pacijenti trebaju kombinirati 1 mg i 3 mg blistera tako da se uzme najmanji broj blistera po dozi (npr., 4 mg doza treba se dati kao jedan 1 mg blister i jedan 3 mg blister). Uzastopna inhalacija tri blistera s jednom dozom od 1 mg rezultira značajno većom izloženošću inzulinu nego udisanje jednog blistera s 3 mg jedinične doze. Stoga tri doze od 1 mg ne smiju biti zamijenjene za jednu dozu od 3 mg (vidjeti KLINIČKA FARMAKOLOGIJA, Farmakokinetika). Kada se pacijent stabilizira na režimu doziranja koji uključuje 3 mg blistera i 3 mg blistera postanu privremeno nedostupni, pacijent može privremeno zamijeniti dva blistera od 1 mg jednim 3 mg žulj. Potrebno je pažljivo nadzirati glukozu u krvi.
Kao i kod svih inzulina, i dodatni faktori koje treba uzeti u obzir pri određivanju početne doze Exubere uključuju, ali nisu ograničeni na pacijentovu trenutnu kontrolu glikemije, prethodni odgovor na inzulin, trajanje dijabetesa, prehranu i vježbanje navike.
Razmatranja titracije doze
Nakon započinjanja liječenja lijekom Exubera, kao i kod drugih sredstava za snižavanje glukoze, možda će biti potrebno prilagođavanje doze na temelju pacijentove potrebe (npr. koncentracije glukoze u krvi, veličina obroka i sastav hranjivih sastojaka, doba dana i nedavno ili očekivano vježba). Svakom pacijentu treba titrirati njegovu optimalnu dozu na temelju rezultata praćenja glukoze u krvi.
Kao i za sve inzuline, vremenski tijek djelovanja Exubera može se razlikovati kod različitih pojedinaca ili u različitom vremenu kod iste jedinke.
Exubera se može koristiti tijekom interkurentnih respiratornih bolesti (npr. Bronhitisa, infekcije gornjih dišnih puteva, rinitisa). Potrebno je usko nadzirati koncentracije glukoze u krvi i prilagoditi dozu na pojedinačnoj osnovi. Inhalirane lijekove (npr. Bronhodilatatore) treba primijeniti prije primjene lijeka Exubera.
vrh
Kako se isporučuje
Exubera (humani inzulin [rDNA porijeklo]) Prašak za inhalaciju dostupan je u blisteru s jediničnom dozom od 1 mg i 3 mg. Blister se izdaje na perforiranim karticama od šest blistera s jednom jediničnom dozom (PVC / aluminij). Dvije jačine se razlikuju po otisku u boji i taktilnim oznakama koje se mogu razlikovati dodirom. Blister od 1 mg i odgovarajuće perforirane kartice ispisani su zelenom tintom, a kartice su označene jednom podignutom trakom. Blister od 3 mg i odgovarajuće perforirane kartice ispisani su plavom tintom, a kartice su označene s tri podignute šipke.
Pet blister karata pakirano je u prozirnu plastičnu (PET) termoformiranu ladicu. Svaka PET ladica također sadrži sredstvo za isušivanje i prekriveno je prozirnim plastičnim (PET) poklopcem. Uložak s pet blister karata (30 blistera s jednom dozom) zapečaćen je u vrećici od laminata s folijom s sredstva za sušenje.
Exubera (humani inzulin [rDNA porijeklo]) Inhalacijski prašak u mjehurićima, Exubera® Inhaler i zamjenski Exubera® Jedinice za puštanje potrebne su za započinjanje terapije lijekom Exubera i nalaze se u paketu Exubera. Potpuno sastavljena Exubera® Inhaler se sastoji od baze za inhalatore, komore i Exubere® Jedinica za puštanje Potpuno sastavljeni Inhaler isporučuje se s zamjenskom komorom, a dostupan je u paketu Exubera i kao zasebna cjelina. Komora je dostupna i kao pojedinačna komponenta.
Exubera® Jedinice za otpuštanje pojedinačno se pakiraju u zatvorenoj termoformiranoj ladici. Jedna Exubera® Jedinica za oslobađanje uključena je u svaki potpuno sastavljeni inhalator. Dvije dodatne jedinice za izdavanje nalaze se u paketu Exubera i u svakom kombiniranom paketu. Jedinice za izdanje Exubera dostupne su i pojedinačno.
Pogledajte tablice 9 i 10 za opis ovih konfiguracija.
Tablica 9
| Exubera (humani inzulin [rDNA porijeklo]) Prah za inhalaciju dostupan je na sljedeći način: | ||
|---|---|---|
| Opis | Sadržaj | NDC |
| Exubera KIT | 1 Exubera Inhaler 1 zamjenska komora 1 mg ~ 180 blistera 3 mg à 90 blistera 2 Exubera® Otpustite jedinice |
0069-0050-85 |
| Exubera kombinirani paket 12 | 1 mg ≥ 90 blistera 3 mg à 90 blistera 2 Exubera® Otpustite jedinice |
0069-0050-19 |
| Exubera kombinirani paket 15 | 1 mg ~ 180 blistera 3 mg à 90 blistera 2 Exubera® Otpustite jedinice |
0069-0050-53 |
| Exubera 1 mg pakiranje za pacijente | 90 — 1 mg 2 Exubera® Otpustite jedinice |
0069-0707-37 |
| Exubera 3 mg pakiranje za pacijente | 90 — 3 mg 2 Exubera® Otpustite jedinice |
0069-0724-37 |
Tablica 10
| Exubera® Inhalator i komponente su dostupni kako slijedi: | ||
|---|---|---|
| Opis | Sadržaj | NDC |
| Exubera® Inhaler i komora | 1 Exubera® Inhalator 1 zamjenska komora |
0069-0054-19 |
| Exubera® Otpustite jedinice | 2 Exubera® Otpustite jedinice | 0069-0097-41 |
| Exubera® Komora | 1 zamjenska komora | 0069-0061-19 |
Spremanje blistera
Ne koristi se (Neotvoreno): Čuvati na kontroliranoj sobnoj temperaturi, 25 ° C (77 ° F); izleti dopušteni na 15-30 ° C [vidi USP kontrolirana temperatura u sobi]. Ne smrzavajte se. Ne hladite.
Tijekom uporabe: Nakon otvaranja omotača folije, mjehurići s jediničnom dozom trebaju se zaštititi od vlage, skladištiti na 25 ° C (77 ° F); izleti dopušteni na 15-30 ° C [vidi USP kontrolirana temperatura u sobi]. Ne smrzavajte se. Ne hladite. Blister s jediničnom dozom treba upotrijebiti u roku od 3 mjeseca nakon otvaranja omota folije. Vratite mjehuriće u omotač da biste zaštitili od vlage. Potrebno je paziti na izbjegavanje vlažnih okruženja, npr. parna kupaonica nakon tuširanja.
Ako su zamrznuti, blister se odbaci.
Skladištenje inhalatora
Čuvati na kontroliranoj sobnoj temperaturi, 25 ° C (77 ° F); izleti dopušteni na 15-30 ° C [vidi USP kontrolirana temperatura u sobi]. Ne smrzavajte se. Ne hladite.
The Exubera® Inhaler se može koristiti najviše 1 godinu od datuma prve upotrebe.
Zamjena Exubera® Jedinica za puštanje
The Exubera® Jedinica za puštanje u Exuberu® Inhaler treba mijenjati svaka 2 tjedna.
Čuvati izvan dohvata djece
Samo Rx

LAB-0331-12,0
zadnja revizija 04/2008
Exubera, humani inzulin [rDNA porijeklo] Podaci o pacijentu (na običnom engleskom)
Detaljne informacije o znakovima, simptomima, uzrocima, liječenjima dijabetesa
Podaci u ovoj monografiji nisu namijenjeni pokrivanju svih mogućih upotreba, uputa, mjera opreza, interakcija lijekova ili štetnih učinaka. Ovi podaci su generalizirani i nisu zamišljeni kao posebni medicinski savjeti. Ako imate pitanja o lijekovima koje uzimate ili želite više informacija, obratite se svom liječniku, ljekarniku ili medicinskoj sestri.
natrag na: Pregledajte sve lijekove za dijabetes


