Glukofag za liječenje dijabetesa
Robna marka: Glucophage
Generičko ime: metformin hidroklorid
Oblik doziranja: tablete s produljenim oslobađanjem
Sadržaj:
Opis
Klinička farmakologija
Indikacije i upotreba
kontraindikacije
Upozorenja
Mjere opreza
Interakcije s lijekovima
Nuspojave
Predozirati
doza
nabavlja
Glukohage, metformin hidroklorid, podaci o pacijentu (na običnom engleskom)
Opis
Glucophage® (metformin hidroklorid) Tablete i Glucophage® XR (metformin hidroklorid) Tablete s produljenim oslobađanjem su oralni antihiperglikemijski lijekovi koji se koriste u liječenju dijabetesa tipa 2. Metformin hidroklorid (N, N-dimetilimidodikarbonimidni diamid hidroklorid) nije kemijski ili farmakološki povezan s bilo kojom drugom vrstom oralnih antihiperglikemijskih sredstava. Strukturna formula je prikazana:
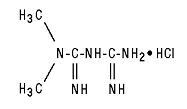
Metformin hidroklorid je bijeli do gotovo bijeli kristalni spoj s molekularnom formulom C4H11N5 - HCl i molekulskom masom od 165,63. Metformin hidroklorid je slobodno topiv u vodi i gotovo netopljiv u acetonu, eteru i kloroformu. PKa metformina je 12,4. PH 1% vodene otopine metformin hidroklorida je 6,68.
Tablete glukofaga sadrže 500 mg, 850 mg ili 1000 mg metformin hidroklorida. Svaka tableta sadrži neaktivne sastojke povidon i magnezijev stearat. Pored toga, obloga za tablete od 500 mg i 850 mg sadrži hipromelozu, a obloga za tabletu od 1000 mg sadrži hipromelozu i polietilen glikol.
Glukofag XR sadrži 500 mg ili 750 mg metformin hidroklorida kao aktivnog sastojka.
Glukofag XR tablete od 500 mg sadrže neaktivne sastojke natrijevu karboksimetil celulozu, hipromelozu, mikrokristalnu celulozu i magnezijev stearat.
Glukofag XR tablete od 750 mg sadrže neaktivne sastojke natrijevu karboksimetil celulozu, hipromelozu i magnezijev stearat.
Dijelovi sustava i performanse-Glucophage XR sadrži dvostruki hidrofilni polimerni matrični sustav. Metformin hidroklorid kombinira se s polimerom koji kontrolira otpuštanje lijeka, čime se formira "unutarnja" faza, koja se zatim uključuje kao diskretne čestice u "vanjsku" fazu drugog polimera. Nakon primjene, tekućina iz gastrointestinalnog (GI) trakta ulazi u tabletu, zbog čega polimeri hidriraju i nabubre. Lijek se oslobađa iz doznog oblika postupkom difuzije kroz gel matricu koja je u osnovi neovisna o pH. Hidrirani polimerni sustav nije krut i očekuje se da će ga razbiti normalna peristaltika u GI traktu. Biološki inertne komponente tablete mogu povremeno ostati netaknute tijekom GI tranzita i biti će eliminirane u izmetu kao meka, hidrirana masa.
vrh
Klinička farmakologija
Mehanizam djelovanja
Metformin je antihiperglikemijsko sredstvo koje poboljšava toleranciju na glukozu u bolesnika s dijabetesom tipa 2, snižavajući bazalnu i postprandialnu glukozu u plazmi. Njegovi farmakološki mehanizmi djelovanja razlikuju se od ostalih klasa oralnih antihiperglikemijskih sredstava. Metformin smanjuje proizvodnju glukoze u jetri, smanjuje crijevnu apsorpciju glukoze i poboljšava osjetljivost na inzulin povećavajući periferni unos i iskorištavanje glukoze. Za razliku od sulfonilureje, metformin ne proizvodi hipoglikemiju ni u bolesnika s dijabetesom tipa 2, ni kod normalnih ispitanika (osim u posebnim okolnostima, vidi MJERE OPREZA) i ne uzrokuje hiperinzulinemiju. Uz terapiju metforminom, izlučivanje inzulina ostaje nepromijenjeno, dok nivo inzulina na vrijeme i cjeloživotni odgovor na inzulin u plazmi mogu zapravo opadati.
farmakokinetika
Apsorpcija i bioraspoloživost
Apsolutna bioraspoloživost tablete Glucophage 500 mg koja se daje u uvjetima posta je oko 50% do 60%. Studije koje koriste pojedinačne oralne doze glukofaga od 500 do 1500 mg i 850 do 2550 mg pokazuju da nedostaje proporcionalnost doze s povećanjem doza, što zbog smanjene apsorpcije, a ne promjene u eliminacije. Hrana smanjuje opseg i malo odlaže apsorpciju metformina, što pokazuje otprilike 40% niži prosječni vrh plazme koncentracija (Cmax), 25% niža površina ispod koncentracije plazme u odnosu na vremensku krivulju (AUC) i produženje vremena do vrhunca za 35 minuta koncentracija u plazmi (Tmax) nakon primjene jedne 850 mg tablete metformina s hranom, u usporedbi s istom jačinom tablete postivano post. Klinička važnost ovih smanjenja nije poznata.
Nakon pojedinačne oralne doze glukofaga XR, Cmax se postiže s srednjom vrijednošću od 7 sati i rasponom od 4 do 8 sati. Najviša razina u plazmi približno je 20% niža u usporedbi s istom dozom glukofaga, međutim, stupanj apsorpcije (mjereno AUC-om) sličan je glukofagu.
U stanju pripravnosti, AUC i Cmax manji su od proporcionalne doze za Glucophage XR u rasponu od 500 do 2000 mg primijenjenih jednom dnevno. Najviša razina u plazmi iznosi otprilike 0,6, 1,1, 1,4 i 1,8 µg / ml za doze od 500, 1000, 1500 i 2000 mg jednom dnevno. Opseg apsorpcije metformina (mjereno AUC-om) iz glukofaga XR u dozi od 2000 mg jednom dnevno sličan je istoj ukupnoj dnevnoj dozi primijenjenoj kao tablete glukofaga 1000 mg dva puta dnevno. Nakon opetovane primjene glukofaga XR, metformin se nije nakupljao u plazmi.
Varijabilnost unutar subjekta u Cmaxu i AUC metformina iz Glucophage XR usporediva je s onom glukofaga.
Iako je opseg apsorpcije metformina (mjereno AUC) iz Glucophage XR tablete povećana za oko 50% kada se daje s hranom, nije bilo utjecaja hrane na Cmax i Tmax od metformin. Obrok s visokim i niskim udjelom masti imao je isti učinak na farmakokinetiku glukofaga XR.
Distribucija
Prividni volumen distribucije (V / F) metformina nakon pojedinačnih oralnih doza glukofaga 850 mg u prosjeku je iznosio 654 ± 358 L. Metformin se zanemarivo veže na proteine plazme, za razliku od sulfonilureje, koji su vezani za više od 90% proteina. Podjele metformina u eritrocite, najvjerojatnije kao funkcija vremena. U uobičajenim kliničkim dozama i rasporedima doziranja glukofaga, stalne koncentracije metformina u plazmi dosežu se u roku od 24 do 48 sati i obično su
Metabolizam i eliminacija
Intravenske studije s jednom dozom kod normalnih ispitanika pokazuju da se metformin izlučuje nepromijenjen u urin i ne podliježe jetrenom metabolizmu (kod ljudi nisu utvrđeni metaboliti) niti bilijarnom izlučivanje. Bubrežni klirens (vidi stol 1) približno je 3,5 puta veći od klirensa kreatinina, što ukazuje da je tubulna sekrecija glavni put eliminacije metformina. Nakon oralne primjene, otprilike 90% apsorbiranog lijeka eliminira se putem bubrega u prva 24 sata, s poluživotom eliminacije iz plazme od približno 6,2 sata. Poluživot eliminacije u krvi je otprilike 17,6 sati, što sugerira da masa eritrocita može biti odjeljak raspodjele.
Posebne populacije
Pacijenti s dijabetesom tipa 2
U prisutnosti normalne funkcije bubrega, ne postoje razlike između farmakokinetike metformina s jednom ili više doza između pacijenata s dijabetesom tipa 2 i normalnih ispitanika (vidjeti stol 1) niti se nakuplja metformin u bilo kojoj skupini u uobičajenim kliničkim dozama.
Farmakokinetika glukofaga XR u bolesnika s dijabetesom tipa 2 usporediva je s onima u zdravih normalnih odraslih.
Bubrežna insuficijencija
U bolesnika sa smanjenom bubrežnom funkcijom (na temelju izmjerenog klirensa kreatinina), poluživot plazme i krvi metformin se produžuje, a bubrežni klirens smanjuje se proporcionalno smanjenju klirensa kreatinina (vidi stol 1; također vidjeti UPOZORENJA).
Jetrna insuficijencija
Nikakva farmakokinetička ispitivanja metformina nisu provedena u bolesnika s hepatičkom insuficijencijom.
Gerijatrija
Ograničeni podaci iz kontroliranih farmakokinetičkih ispitivanja glukofaga u zdravih starijih ispitanika sugeriraju da je ukupna plazma očistenje metformina je smanjeno, poluživot je produžen, a Cmax je povećan, u usporedbi sa zdravim mladima subjekti. Iz tih podataka proizlazi da se promjena farmakokinetike metformina sa starenjem primarno objašnjava promjenom bubrežne funkcije (vidi stol 1). Glukofag (metformin hidroklorid) Tablete i glukofag XR (metformin hidroklorid) Tablete s produljenim oslobađanjem ne bi trebale započinje s pacijentima starim 80 godina, osim ako mjerenje klirensa kreatinina ne pokaže da bubrežna funkcija nije smanjena (vidjeti UPOZORENJA i DOZIRANJE I UPRAVLJANJE).
Tablica 1: Odaberite srednje (± S.D.) Farmakokinetičke parametre metformina nakon pojedinačnih ili višestrukih oralnih doza glukofaga
| Grupe predmeta: Doza glukofaga (broj predmeta) |
Cmaksimumb (µg / mL) |
Tmaksimumc (h) |
Bubrežni čišćenje (Ml / min) |
|---|---|---|---|
| Sve se doze daju na teret osim prvih 18 doza ispitivanja višestrukih doza | |||
| b Najviša koncentracija u plazmi | |||
| c Vrijeme do vršne koncentracije u plazmi | |||
| d Kombinirani rezultati (prosjek prosjeka) pet studija: prosječna dob 32 godine (raspon 23-59 godina) | |||
| e Kinetička studija izvedena nakon doze 19, nakon posta | |||
| f Stariji ispitanici, prosječna dob 71 godina (raspon 65-81 godina) | |||
| g CLcr = klirens kreatinina normaliziran na površini tijela 1,73 m2 | |||
| Zdrave, nedijabetične odrasle osobe: | |||
| 500 mg pojedinačna doza (24) | 1.03 ( ±0.33) | 2.75 ( ±0.81) | 600 ( ±132) |
| 850 mg pojedinačna doza (74)d | 1.60 ( ±0.38) | 2.64 ( ±0.82) | 552 ( ±139) |
| 850 mg tri puta dnevno tijekom 19 dozae (9) | 2.01 ( ±0.42) | 1.79 ( ±0.94) | 642 ( ±173) |
| Odrasli s dijabetesom tipa 2: | |||
| 850 mg pojedinačna doza (23) | 1.48 ( ±0.5) | 3.32 ( ±1.08) | 491 ( ±138) |
| 850 mg tri puta dnevno tijekom 19 dozae (9) | 1.90 ( ±0.62) | 2.01 ( ±1.22) | 550 ( ±160) |
| postarijif, zdrave odrasle osobe bez dijabetesa: | |||
| 850 mg pojedinačna doza (12) | 2.45 ( ±0.70) | 2.71 ( ±1.05) | 412 ( ±98) |
| Odrasli s oštećenjem bubrega: | |||
| Jednostruka doza od 850 mg | |||
| Blaga (CL)crg 61-90 mL / min) (5) | 1.86 ( ±0.52) | 3.20 ( ±0.45) | 384 ( ±122) |
| Umjereno (CL)cr 31-60 ml / min) (4) | 4.12 ( ±1.83) | 3.75 ( ±0.50) | 108 ( ±57) |
| Ozbiljan (CL)cr 10-30 ml / min) (6) | 3.93 ( ±0.92) | 4.01 ( ±1.10) | 130 ( ±90 |
pedijatrija
Nakon primjene pojedinačne oralne tablete glukofaga od 500 mg s hranom, srednja geometrijska vrijednost Cmax metformina i AUC razlikovala se manje od 5% pedijatrijski bolesnici s dijabetesom tipa 2 (u dobi od 12-16 godina) i zdrave odrasle osobe (20-45 godina) s rokom i težinom, svi sa normalnom renalnom bolešću funkcija
rod
Farmakokinetički parametri metformina nisu se značajno razlikovali između normalnih ispitanika i bolesnika s dijabetesom tipa 2 kada su analizirani prema spolu (muškarci = 19, žene = 16). Slično tome, u kontroliranim kliničkim studijama u bolesnika s dijabetesom tipa 2, antihiperglikemijski učinak glukofaga bio je usporediv u muškaraca i žena.
utrka
Nisu provedena ispitivanja farmakokinetičkih parametara metformina prema rasi. U kontroliranim kliničkim studijama glukofaga u bolesnika s dijabetesom tipa 2, antihiperglikemijski učinak bio je usporediv kod bijelaca (n = 249), crnaca (n = 51) i latinoamerikanaca (n = 24).
Kliničke studije
Glucophage
U dvostruko slijepom, placebo kontroliranom, višecentričnom američkom kliničkom ispitivanju koje je uključivalo pretile bolesnike s dijabetesom tipa 2 čija hiperglikemija nije bila adekvatno kontrolirana s samostalno upravljanje prehranom (početna glukoza u plazmi natašte [FPG] od približno 240 mg / dL), liječenje glukofagom (do 2550 mg / dan) tijekom 29 tjedana rezultiralo je značajnim srednje neto smanjenje glukoze u plazmi nakon posta i postprandijalne glukoze (PPG) i hemoglobina A1c (HbA1c) od 59 mg / dL, 83 mg / dL, odnosno 1,8%, u usporedbi s placebo skupinom (vidjeti Tablica 2).
Tablica 2: Glukofag vs placebo sažetak srednjih promjena od osnovne vrijednosti * u glukozi u plazmi nakon posta, HbA1ci tjelesna težina u završnom posjetu (studija u 29 tjedana)
| Glucophage (N = 141) |
Placebo (N = 145) |
p-vrijednost | |
|---|---|---|---|
| * Svi pacijenti na dijetnoj terapiji na bazi | ** Nije statistički značajno | ||
| FPG (mg / dL) Osnovna linija Promjena u FINAL VISIT |
241.5 -53.0 |
237.7 6.3 |
NS ** 0.001 |
| Hemoglobin A1c (%) Osnovna linija Promjena u FINAL VISIT |
8.4 -1.4 |
8.2 0.4 |
NS ** 0.001 |
| Tjelesna težina (lbs) Osnovna linija Promjena u FINAL VISIT |
201.0 -1.4 |
206.0 -2.4 |
NS ** NS ** |
Dvostruko slijepo, placebo kontrolirano ispitivanje glukofaga i gliburida, 29 i tjedno, provedeno u bolesnika s pretilim tipom 2 dijabetes koji nije uspio postići odgovarajuću glikemijsku kontrolu dok je bio na maksimalnim dozama glikurida (početni FPG od približno 250 mg / dL) (vidjeti tablicu 3). Pacijenti randomizirani u kombinirani krak započeli su terapiju glukofagom 500 mg i gliburidom 20 mg. Na kraju svakog tjedna u prva 4 tjedna ispitivanja, ovim pacijentima doziranje glukofaga povećavalo se za 500 mg, ako nisu uspjeli postići ciljnu glukozu u plazmi. Nakon 4. tjedna, takve su prilagodbe doze vršene mjesečno, mada niti jednom pacijentu nije dopušteno prekoračenje 2500 mg glukofaga. Pacijenti u skupini koja je primala samo glukofage (metformin plus placebo) slijedili su isti raspored titracije. Na kraju ispitivanja, otprilike 70% bolesnika u kombiniranoj skupini uzimalo je Glucophage 2000 mg / gliburid 20 mg ili Glucophage 2500 mg / gliburid 20 mg. Pacijenti randomizirani za nastavak primjene gliburida doživjeli su pogoršanje kontrole glikemije, s srednjim porastom FPG, PPG i HbA1c od 14 mg / dL, 3 mg / dL, odnosno 0,2%. Nasuprot tome, oni randomizirani u glukofag (do 2500 mg / dan) doživjeli su neznatno poboljšanje, sa srednjim smanjenjem FPG, PPG i HbA1c od 1 mg / dL, 6 mg / dL, odnosno 0,4%. Kombinacija glukofaga i gliburida bila je učinkovita u smanjenju razine FPG, PPG i HbA1c za 63 mg / dL, 65 mg / dL, odnosno 1,7%. U usporedbi s rezultatima samoga liječenja gliburidom, neto razlike kod kombiniranog liječenja bile su -77 mg / dL, -68 mg / dL, odnosno -1,9%, (respektivno, vidjeti tablicu 3).
Tablica 3: Monoterapija kombiniranog glukofaga / gliburida (češalj) vs gliburida (glyb) ili glukofaga (GLU): sažetak prosječnih promjena od osnovne vrijednosti * u glukozi u plazmi na tešče, HbA1ci tjelesna težina u završnom posjetu (studija u 29 tjedana)
| p-vrijednosti | ||||||
|---|---|---|---|---|---|---|
| Češalj (N = 213) |
Glyb (N = 209) |
GLU (N = 210) |
Glyb vs Češalj |
GLU vs Češalj |
GLU vs Glyb |
|
| * Svi pacijenti koji su uzimali gliburid, 20 mg / dan, u osnovnoj fazi | ** Nije statistički značajno | |||||
| Plazma glukoza nakon posta (mg / dL) | ||||||
| Osnovna linija Promjena u FINAL VISIT |
250.5 -63.5 |
247.5 13.7 |
253.9 -0.9 |
NS ** 0.001 |
NS ** 0.001 |
NS ** 0.025 |
| Hemoglobin A1c (%) | ||||||
| Osnovna linija Promjena u FINAL VISIT |
8.8 -1.7 |
8.5 0.2 |
8.9 -0.4 |
NS ** 0.001 |
NS ** 0.001 |
0.007 0.001 |
| Tjelesna težina (lbs) | ||||||
| Osnovna linija Promjena u FINAL VISIT |
202.2 0.9 |
203.0 -0.7 |
204.0 -8.4 |
NS ** 0.011 |
NS ** 0.001 |
NS ** 0.001 |
Stupanj pada koncentracije glukoze u krvi na glasu nakon ustanove Terapija glukofagom (metforminijevim kloridom) Terapija tabletama bila je proporcionalna razini posta hiperglikemija. Bolesnici s dijabetesom tipa 2 s višom koncentracijom glukoze na glavi imali su veći pad glukoze u plazmi i glikoziliranog hemoglobina.
U kliničkim studijama glukofag, sam ili u kombinaciji sa sulfonilureom, snižavao prosječni serum za gladovanje razine triglicerida, ukupnog kolesterola i LDL kolesterola, a nisu imali štetne učinke na ostale razine lipida (vidjeti Tablica 4).
Tablica 4: Sažetak prosječne promjene u odnosu na početnu vrijednost glavnih serumskih lipidnih varijabli kod završnog posjeta (studije od 29 tjedana)
| Glucophage vs Placebo | Kombinirani glukofag / gliburid vs monoterapija |
||||
|---|---|---|---|---|---|
| Glucophage (N = 141) |
Placebo (N = 145) |
Glucophage (N = 210) |
Glucophage / gliburid (N = 213) |
gliburid (N = 209) |
|
| Ukupni kolesterol (mg / dL) | |||||
| Osnovna linija Srednja% promjene pri konačnom posjetu |
211.0 -5% |
212.3 1% |
213.1 -2% |
215.6 -4% |
219.6 1% |
| Ukupni trigliceridi (mg / dL) | |||||
| Osnovna linija Srednja% promjene pri konačnom posjetu |
236.1 -16% |
203.5 1% |
242.5 -3% |
215.0 -8% |
266.1 4% |
| LDL-kolesterol (mg / dL) | |||||
| Osnovna linija Srednja% promjene pri konačnom posjetu |
135.4 -8% |
138.5 1% |
134.3 -4% |
136.0 -6% |
137.5 3% |
| HDL-kolesterol (mg / dL) | |||||
| Osnovna linija Srednja% promjene pri konačnom posjetu |
39.0 2% |
40.5 -1% |
37.2 5% |
39.0 3% |
37.0 1% |
Za razliku od sulfonilureje, tjelesna težina pojedinaca na glukofagu obično ostaje stabilna ili se čak donekle smanjuje (vidi Tablice 2 i 3).
Dvostruko slijepo, placebo kontrolirano ispitivanje glukofaga plus inzulina u trajanju od 24 tjedna u odnosu na inzulin plus placebo provedeno na pacijentima s dijabetesom tipa 2 koji nisu uspjeli postići odgovarajuću glikemijsku kontrolu samo na inzulinu (vidjeti Tablica 5). Pacijenti randomizirani za primanje glukofaga plus inzulina postigli su smanjenje HbA1c za 2,10%, u usporedbi s smanjenjem HbA1c od 1,56% postignutim inzulinom plus placebom. Poboljšanje kontrole glikemije postignuto je u posljednjem studijskom posjetu sa 16% manje inzulina, 93,0 U / dan u odnosu na 110,6 U / dan, Glukofaga plus inzulina u odnosu na inzulin plus placebo, p = 0,04.
Tablica 5: Kombinirani glukofag / inzulin vs placebo / sažetak inzulina prosječnih promjena od polazne vrijednosti u HbA1c i dnevna doza inzulina
| Glucophage / insulin (N = 26) |
Placebo/ insulin (N = 28) |
liječenje Razlika Srednja vrijednost ± SE |
|
|---|---|---|---|
|
Statistički značajna korištenjem analize kovarijancije s početnom vrijednosti kao kovarijatnom (p = 0,04) Nije značajno korištenjem analize varijance (vrijednosti prikazane u tablici) | |||
| b Statistički značajan za inzulin (p = 0,04) | |||
| Hemoglobin A1c (%) | |||
| Osnovna linija Promjena u FINAL VISIT |
8.95 -2.10 |
9.32 -1.56 |
-0.54 ± 0.43 |
| Doza inzulina (U / dan) | |||
| Osnovna linija Promjena u FINAL VISIT |
93.12 -0.15 |
94.64 15.93 |
-16.08 ± 7.77b |
Druga dvostruko slijepa, placebo kontrolirana studija (n = 51), sa 16 tjedana randomiziranog liječenja, pokazala je da u bolesnika s dijabetesom tipa 2 kontrolirani inzulin tijekom 8 tjedana s prosječnim HbA1c od 7,46 ± 0,97%, dodatak Glucophage održavao je sličnu glikemijsku kontrolu (HbA1c 7,15 ± 0,61 vs 6,97 ± 0,62 za Glucophage plus inzulin i placebo plus inzulina, respektivno) s 19% manje inzulina u odnosu na početnu vrijednost (smanjenje od 23,68 ± 30,22 u usporedbi s porastom od 0,43 ± 25,20 jedinica za Glucophage plus inzulin i placebo plus inzulin, p <0,01). Pored toga, ova studija pokazala je da kombinacija glukofaga i inzulina rezultira smanjenjem tjelesnom težinom od 3,11 ± 4,30 lbs u usporedbi s porastom od 1,30 ± 6,08 funti za placebo plus inzulin, p = 0.01.
Glukofag XR
Provedeno je 24-tjedno dvostruko slijepo placebo kontrolirano istraživanje glukofaga XR, uzeto jednom dnevno uz večernji obrok u bolesnici s dijabetesom tipa 2 koji nisu uspjeli postići glikemijsku kontrolu prehranom i vježbanjem (HbA1c 7,0% -10,0%, FPG 126-270 mg / dL). Pacijenti koji su ušli u studiju imali su prosječnu vrijednost HbA1c od 8,0% i srednju vrijednost FPG od 176 mg / dL. Nakon 12 tjedana liječenja, prosječni HbA1c porastao je od početne vrijednosti za 0,1%, a prosječni FPG se smanjio od početnog za 2 mg / dL u skupini koja je primala placebo, u usporedbi sa smanjenjem prosječnog HbA1c od 0,6% i smanjenjem prosječnog FPG-a od 23 mg / dL u bolesnika liječenih glukofagom XR 1000 mg jednom dnevno. Nakon toga, doza liječenja povećana je na 1500 mg jednom dnevno ako HbA1c iznosi 7,0%, ali <8,0% (bolesnici s HbA1c - 8,0% su prekinuti iz ispitivanja). U posljednjem posjetu (24-tjedan), prosječni HbA1c porastao je 0,2% od početne vrijednosti u bolesnika koji su primali placebo i smanjio se 0,6% s Glucophage XR.
16-tjedno dvostruko slijepo, placebo kontrolirano, ispitivanje doze Glucophage XR, uzeto jednom dnevno uz večernji obrok ili dva puta dnevno uz obroke, je provedeno u bolesnika s dijabetesom tipa 2 koji nisu uspjeli postići glikemijsku kontrolu prehranom i vježbanjem (HbA1c 7,0% -11,0%, FPG 126-280 mg / dL). Promjene u kontroli glikemije i tjelesne težine prikazane su u tablici 6.
Tablica 6: Sažetak srednjih promjena od polazne linije * u HbA1c, Postizanje plazme glukoze i tjelesne težine u posljednjem posjetu (16-tjedno istraživanje)
| Glukofag XR | Placebo | |||||
|---|---|---|---|---|---|---|
| 500 mg Jednom Dnevno |
1000 mg Jednom Dnevno |
1500 mg Jednom Dnevno |
2000 mg Jednom Dnevno |
1000 mg Dvaput Dnevno |
||
| * Svi pacijenti na dijetnoj terapiji na bazi | ||||||
| Sve usporedbe s placebom | ||||||
| ** Nije statistički značajno | ||||||
| Hemoglobin A1c (%) | (N = 115) | (N = 115) | (N = 111) | (N = 125) | (N = 112) | (N = 111) |
| Osnovna linija | 8.2 | 8.4 | 8.3 | 8.4 | 8.4 | 8.4 |
| Promjena u FINAL VISIT | -0.4 | -0.6 | -0.9 | -0.8 | -1.1 | 0.1 |
| p-vrijednost | <0.001 | <0.001 | <0.001 | <0.001 | <0.001 | - |
| FPG (mg / dL) | (N = 126) | (N = 118) | (N = 120) | (N = 132) | (N = 122) | (N = 113) |
| Osnovna linija | 182.7 | 183.7 | 178.9 | 181.0 | 181.6 | 179.6 |
| Promjena u FINAL VISIT | -15.2 | -19.3 | -28.5 | -29.9 | -33.6 | 7.6 |
| p-vrijednost | <0.001 | <0.001 | <0.001 | <0.001 | <0.001 | - |
| Tjelesna težina (lbs) | (N = 125) | (N = 119) | (N = 117) | (N = 131) | (N = 119) | (N = 113) |
| Osnovna linija | 192.9 | 191.8 | 188.3 | 195.4 | 192.5 | 194.3 |
| Promjena u FINAL VISIT | -1.3 | -1.3 | -0.7 | -1.5 | -2.2 | -1.8 |
| p-vrijednost | NS ** | NS ** | NS ** | NS ** | NS ** | - |
U usporedbi s placebom, poboljšanje kontrole glikemije primijećeno je na svim razinama doze glukofaga XR (metformin hidroklorid) Tablete s produljenim oslobađanjem i liječenje nije povezano sa značajnom promjenom težine (vidjeti DOZIRANJE I UPRAVLJANJE za preporuke doziranja za Glucophage i Glucophage XR).
Dvostruko slijepo, nasumično, randomizirano istraživanje glukofaga XR, uzeto jednom dnevno uz večernji obrok, i tablete glukofaga (metformin hidroklorid), uzimaju se dva puta dnevno (sa doručak i večernji obrok), provedeno je kod bolesnika s dijabetesom tipa 2 koji su liječeni glukofagom 500 mg dva puta dnevno najmanje 8 tjedana prije ulaska u studiju. Doza glukofaga nije nužno titrirana kako bi se postigla određena razina kontrole glikemije prije ulaska u studiju. Pacijenti kvalificirani za ispitivanje ako HbA1c iznosi ‰ â 8,5%, a FPG je ‰ â 200 mg / dL. Promjene u kontroli glikemije i tjelesne težine prikazane su u tablici 7.
Tablica 7: Sažetak srednjih promjena od polazne linije * u HbA1c, Postizanje plazme glukoze i tjelesne težine u 12. tjednu i u završnom posjetu (studija od 24 tjedna)
| Glucophage 500 mg Dvaput dnevno |
Glukofag XR | ||
|---|---|---|---|
| 1000 mg Jednom dnevno |
1500 mg Jednom dnevno |
||
| * Svi pacijenti koji su uzimali glukofag 500 mg dva puta dnevno na osnovnoj osnovi | |||
| n = 68 | |||
| Hemoglobin A1c (%) | (N = 67) | (N = 72) | (N = 66) |
| Osnovna linija | 7.06 | 6.99 | 7.02 |
| Promjena u 12 tjedana | 0.14 | 0.23 | 0.04 |
| (95% CI) | (-0.03, 0.31) | (0.10, 0.36) | (-0.08, 0.15) |
| Promjena u FINAL VISIT | 0.14 | 0.27 | 0.13 |
| (95% CI) | (-0.04, 0.31) | (0.11, 0.43) | (-0.02, 0.28) |
| FPG (mg / dL) | (N = 69) | (N = 72) | (N = 70) |
| Osnovna linija | 127.2 | 131.0 | 131.4 |
| Promjena u 12 tjedana | 12.9 | 9.5 | 3.7 |
| (95% CI) | (6.5, 19.4) | (4.4, 14.6) | (-0.4, 7.8) |
| Promjena u FINAL VISIT | 14.0 | 11.5 | 7.6 |
| (95% CI) | (7.0, 21.0) | (4.4, 18.6) | (1.0, 14.2) |
| Tjelesna težina (lbs) | (N = 71) | (N = 74) | (N = 71) |
| Osnovna linija | 210.3 | 202.8 | 192.7 |
| Promjena u 12 tjedana | 0.4 | 0.9 | 0.7 |
| (95% CI) | (-0.4, 1.5) | (0.0, 2.0) | (-0.4, 1.8) |
| Promjena u FINAL VISIT | 0.9 | 1.1 | 0.9 |
| (95% CI) | (-0.4, 2.2) | (-0.2, 2.4) | (-0.4, 2.0) |
Nakon 12 tjedana liječenja, došlo je do povećanja prosječnog HbA1c u svim skupinama; u skupini s Glucophage XR 1000 mg, porast od početne vrijednosti od 0,23% bio je statistički značajan (vidi DOZIRANJE I UPRAVLJANJE).
Promjene lipidnih parametara u prethodno opisanom placebo kontroliranom ispitivanju doze Glucophage XR prikazane su u Tablici 8.
Tablica 8: Sažetak prosječnih promjena u odnosu na osnovnu vrijednost * u glavnim lipidnim varijablama u završnom posjetu (16-tjedno istraživanje)
| Glukofag XR | Placebo | |||||
|---|---|---|---|---|---|---|
| 500 mg Jednom Dnevno |
1000 mg Jednom Dnevno |
1500 mg Jednom Dnevno |
2000 mg Jednom Dnevno |
1000 mg Dvaput Dnevno |
||
| * Svi pacijenti na dijetnoj terapiji na bazi | ||||||
| Ukupni kolesterol (mg / dL) | (N = 120) | (N = 113) | (N = 110) | (N = 126) | (N = 117) | (N = 110) |
| Osnovna linija | 210.3 | 218.1 | 214.6 | 204.4 | 208.2 | 208.6 |
| Srednja% promjene pri konačnom posjetu | 1.0% | 1.7% | 0.7% | -1.6% | -2.6% | 2.6% |
| Ukupni trigliceridi (mg / dL) | (N = 120) | (N = 113) | (N = 110) | (N = 126) | (N = 117) | (N = 110) |
| Osnovna linija | 220.2 | 211.9 | 198.0 | 194.2 | 179.0 | 211.7 |
| Srednja% promjene pri konačnom posjetu | 14.5% | 9.4% | 15.1% | 14.9% | 9.4% | 10.9% |
| LDL-kolesterol (mg / dL) | (N = 119) | (N = 113) | (N = 109) | (N = 126) | (N = 117) | (N = 107) |
| Osnovna linija | 131.0 | 134.9 | 135.8 | 125.8 | 131.4 | 131.9 |
| Srednja% promjene pri konačnom posjetu | -1.4% | -1.6% | -3.5% | -3.3% | -5.5% | 3.2% |
| HDL-kolesterol (mg / dL) | (N = 120) | (N = 108) | (N = 108) | (N = 125) | (N = 117) | (N = 108) |
| Osnovna linija | 40.8 | 41.6 | 40.6 | 40.2 | 42.4 | 39.4 |
| Srednja% promjene pri konačnom posjetu | 6.2% | 8.6% | 5.5% | 6.1% | 7.1% | 5.8% |
Promjene lipidnih parametara u prethodno opisanom ispitivanju glukofaga i glukofaga XR prikazane su u tablici 9.
Tablica 9: Sažetak prosječnih promjena u odnosu na polaznu vrijednost * u glavnim lipidnim varijablama u završnom posjetu (studija od 24 tjedna)
| Glucophage | Glukofag XR | ||
|---|---|---|---|
| 500 mg Dvaput dnevno |
1000 mg Jednom dnevno |
1500 mg Jednom dnevno |
|
| * Svi pacijenti koji su uzimali glukofag 500 mg dva puta dnevno na osnovnoj osnovi | |||
| Ukupni kolesterol (mg / dL) | (N = 68) | (N = 70) | (N = 66) |
| Osnovna linija | 199.0 | 201.9 | 201.6 |
| Srednja% promjene pri konačnom posjetu | 0.1% | 1.3% | 0.1% |
| Ukupni trigliceridi (mg / dL) | (N = 68) | (N = 70) | (N = 66) |
| Osnovna linija | 178.0 | 169.2 | 206.8 |
| Srednja% promjene pri konačnom posjetu | 6.3% | 25.3% | 33.4% |
| LDL-kolesterol (mg / dL) | (N = 68) | (N = 70) | (N = 66) |
| Osnovna linija | 122.1 | 126.2 | 115.7 |
| Srednja% promjene pri konačnom posjetu | −1.3% | −3.3% | −3.7% |
| HDL-kolesterol (mg / dL) | (N = 68) | (N = 70) | (N = 65) |
| Osnovna linija | 41.9 | 41.7 | 44.6 |
| Srednja% promjene pri konačnom posjetu | 4.8% | 1.0% | -2.1% |
Pedijatrijske kliničke studije
U dvostruko slijepom, placebo kontroliranom istraživanju u pedijatrijskih bolesnika u dobi od 10 do 16 godina s dijabetesom tipa 2 (prosječni FPG 182,2 mg / dL), liječenje glukofagom (do 2000. mg / dan) do 16 tjedana (prosječno trajanje liječenja 11 tjedana) rezultiralo je značajnim srednjim neto smanjenjem FPG-a od 64,3 mg / dL, u usporedbi s placebom (vidjeti tablicu 10).
Tablica 10: Glukofag vs placebo (Pedijatrija)) Sažetak prosječnih promjena * od osnovne * u glukozi u plazmi i tjelesnoj težini pri završnom posjetu
| Glucophage | Placebo | p-vrijednost | |
|---|---|---|---|
| Pedijatrijski bolesnici prosječna su dob 13,8 godina (raspon 10-16 godina) | |||
| * Svi pacijenti na dijetnoj terapiji na bazi | |||
| ** Nije statistički značajno | |||
| FPG (mg / dL) | (N = 37) | (N = 36) | |
| Osnovna linija Promjena u FINAL VISIT |
162.4 -42.9 |
192.3 21.4 |
<0.001 |
| Tjelesna težina (lbs) | (N = 39) | (N = 38) | |
| Osnovna linija Promjena u FINAL VISIT |
205.3 -3.3 |
189.0 -2.0 |
NS ** |
vrh
Indikacije i upotreba
Glukofag (metformin hidroklorid) Tablete su indikovane kao dodatak prehrani i vježbanju radi poboljšanja kontrole glikemije u odraslih i djece sa šećernom bolešću tipa 2.
Glukofag XR (metformin hidroklorid) Tablete s produljenim oslobađanjem indicirane su kao dodatak prehrani i tjelovježbi za poboljšanje kontrole glikemije u odraslih s dijabetesom melitusa tipa 2.
vrh
kontraindikacije
Glukofag i Glucophage XR su kontraindicirani u bolesnika sa:
Bubrežna bolest ili bubrežna disfunkcija (npr., Kako to sugeriraju razine kreatinina u serumu ‰ ¥ 1,5 mg / dL [muškarci], ¥ ‰ 1,4 mg / dL [žene] ili abnormalno klirens kreatinina) koji također može biti posljedica stanja poput kardiovaskularnog kolapsa (šok), akutnog infarkta miokarda i septikemije (vidjeti UPOZORENJA i MJERE OPREZA).
Poznata preosjetljivost na metformin hidroklorid.
Akutna ili kronična metabolička acidoza, uključujući dijabetičku ketoacidozu, sa ili bez kome. Dijabetičku ketoacidozu treba liječiti inzulinom.
Glukofage i Glucophage XR treba privremeno prekinuti u bolesnika koji su podvrgnuti radiološkim studijama koje uključuju intravaskularna primjena jodiranih kontrastnih materijala, jer upotreba takvih proizvoda može rezultirati akutnom izmjenom bubrežna funkcija. (Vidi također MJERE OPREZA.)
vrh
Upozorenja
Mliječna acidoza:
Laktacidoza je rijetka, ali ozbiljna metabolička komplikacija koja može nastati zbog nakupljanja metformina tijekom liječenja glukofagom ili glukofagom XR; kada se dogodi, fatalno je otprilike u 50% slučajeva. Laktacidoza se također može pojaviti zajedno s nizom patofizioloških stanja, uključujući dijabetes melitus, i kad god postoji značajna tkivna hipoperfuzija i hipoksemija. Laktacidozu karakteriziraju povišena razina laktata u krvi (> 5 mmol / L), sniženi pH u krvi, poremećaji elektrolita s povećanim jazom aniona i povećani omjer laktata / piruvata. Kad je metformin uzrokovan laktacidozom, obično se nalaze razine plazme metformina> 5 µg / mL.
Prijavljena učestalost laktacidoze u bolesnika koji su primali metformin hidroklorid vrlo je mala (otprilike 0,03 slučaja / 1000 pacijentskih godina, s oko 0,015 smrtnih slučajeva / 1000 Pacijent godina). U više od 20 000 pacijenata tijekom godina izloženosti metforminu u kliničkim ispitivanjima, nije bilo izvještaja o laktacidozi. Prijavljeni slučajevi pojavili su se uglavnom kod dijabetičara sa značajnom bubrežnom insuficijencijom, uključujući oba unutarnja bubrega bolesti i bubrežne hipoperfuzije, često u postavljanju više istodobnih medicinskih / kirurških problema i višestrukih popratnih lijekovi. Bolesnici s kongestivnim zatajenjem srca koji zahtijevaju farmakološko liječenje, osobito oni s nestabilnom ili akutne kongestivne srčane insuficijencije kojima prijeti hipoperfuzija i hipoksemija, povećana je opasnost od laktacije acidoza. Rizik od laktične acidoze povećava se stupnjem bubrežne disfunkcije i dobi pacijenta. Rizik od laktacidoze može se, dakle, značajno smanjiti redovitim nadziranjem bubrežne funkcije u pacijenti koji uzimaju Glucophage ili Glucophage XR i primjenom minimalne učinkovite doze glukofaga ili glukofaga XR. Konkretno, liječenje starijih osoba treba pratiti pažljivo nadziranje bubrežne funkcije. Liječenje glukofagom ili Glucophage XR ne smije se započeti u bolesnika starijih od 80 godina osim ako nije izmjereno kreatinin klirens pokazuje da se bubrežna funkcija ne smanjuje, jer su ti bolesnici osjetljiviji na razvoj lakta acidoza. Povrh toga, glukofage i glukofage XR potrebno je brzo odustati u prisustvu bilo kojeg stanja povezanog s hipoksemijom, dehidracijom ili sepsom. Budući da oštećena jetrena funkcija može značajno ograničiti sposobnost čišćenja laktata, glukofaga i Glukofag XR treba općenito izbjegavati u bolesnika s kliničkim ili laboratorijskim dokazima jetre bolest. Bolesnike treba upozoriti na prekomjerni unos alkohola, bilo akutnog ili kroničnog, tijekom uzimanja Glukofag ili Glucophage XR, jer alkohol pojačava učinke metformin hidroklorida na laktat metabolizam. Uz to, Glucophage i Glucophage XR moraju se privremeno obustaviti prije bilo kojeg intravaskularnog radiokontrastnog ispitivanja i bilo kojeg kirurškog zahvata (vidjeti također MJERE OPREZA).
Pojava laktične acidoze često je suptilna i popraćena je samo nespecifičnim simptomima kao što su nelagoda, mialgije, respiratorni distres, povećanje somnolencije i nespecifični trbušni nevolje. Može postojati povezana hipotermija, hipotenzija i rezistentne bradiaritmije s izraženijom acidozom. Pacijent i pacijentov liječnik moraju biti svjesni moguće važnosti takvih simptoma, a pacijentu treba uputiti da odmah obavijesti liječnika ako se pojave (vidi također MJERE OPREZA). Glukofage i Glucophage XR treba povući dok se situacija ne razjasni. Elektroliti u serumu, ketoni, glukoza u krvi i ako je naznačeno, pH u krvi, razini laktata, pa čak i razine metformina u krvi mogu biti korisni. Jednom kada se pacijent stabilizira na bilo kojoj razini doze glukofaga ili glukofaga XR, gastrointestinalni simptomi koji su uobičajeni tijekom započinjanja terapije vjerojatno neće biti povezani s lijekovima. Kasnija pojava gastrointestinalnih simptoma može biti posljedica laktacidoze ili druge ozbiljne bolesti.
Razine laktata venske plazme na glavi iznad gornje granice normalne, ali manje od 5 mmol / L u bolesnika koji uzimaju glukofag ili glukofag XR ne moraju nužno naznačiti predstojeća laktacidoza, a može se objasniti drugim mehanizmima, poput loše kontroliranog dijabetesa ili pretilosti, snažne fizičke aktivnosti ili tehničkih problema u uzorku rukovanje. (Vidi također MJERE OPREZA.)
Laktacidoza treba posumnjati u bilo kojeg bolesnika s dijabetesom s metaboličkom acidozom koja nema dokaza o ketoacidozi (ketonurija i ketonemija).
Laktacidoza je hitna medicinska pomoć koja se mora liječiti u bolničkim uvjetima. U bolesnika s laktacidozom koji uzimaju Glucophage ili Glucophage XR, lijek treba odmah prekinuti i odmah započeti s općim potpornim mjerama. Budući da se metformin hidroklorid može dijalizirati (klirens do 170 ml / min, pod dobrim hemodinamičkim stanja), preporučuje se brza hemodijaliza za ispravljanje acidoze i uklanjanje nakupljene metformin. Takvo upravljanje često rezultira brzim ukidanjem simptoma i oporavkom. (Vidi također KONTRAINDIKACIJE i MJERE OPREZA.)
vrh
Mjere opreza
Općenito
Makrovaskularni ishodi - Nijedna klinička studija nije utvrdila dokaze o smanjenju makrovaskularnog rizika s glukofagom ili glukofagom XR ili bilo kojim drugim antidijabetičkim lijekom.
Nadziranje bubrežne funkcije - Znano je da se metformin uglavnom izlučuje putem bubrega i rizik od nakupljanja metformina i laktacidoza raste sa stupnjem oštećenja bubrega funkcija. Stoga bolesnici s razinom kreatinina u serumu iznad gornje granice normale za svoju dob ne smiju primati glukofage ili glukofage XR. U bolesnika u poodmakloj dobi potrebno je pažljivo titrirati Glucophage i Glucophage XR kako bi se utvrdili minimalna doza za odgovarajući glikemijski učinak, jer je starenje povezano sa smanjenim renalnim funkcija. U starijih bolesnika, osobito onih u dobi od 80 godina, bubrežnu funkciju treba redovito nadzirati, i općenito, glukofag i glukofag XR ne smiju biti titrirani do maksimalne doze (vidjeti UPOZORENJA i DOZIRANJE I UPRAVLJANJE).
Prije početka liječenja glukofagom ili glukofagom XR i najmanje jednom godišnje nakon toga, bubrežnu funkciju treba procijeniti i provjeriti kao normalnu. U bolesnika kod kojih se predviđa razvoj bubrežne disfunkcije, potrebno je procijeniti bubrežnu funkciju češće i Glucophage ili Glucophage XR se obustavljaju ako postoje dokazi o oštećenju bubrega predstaviti.
Upotreba istodobnih lijekova koji mogu utjecati na bubrežnu funkciju ili dispoziciju metformina - Istodobni lijekovi koji mogu utjecati na bubrežnu funkciju ili rezultirati u značajna hemodinamička promjena ili može ometati dispoziciju metformina, poput kationskih lijekova koji se uklanjaju bubrežnom tubularnom sekrecijom (vidjeti MJERE OPREZA: Interakcije lijekova), treba koristiti s oprezom.
Radiološke studije koje uključuju upotrebu kontrastnih materijala s jodiranim jodom (na primjer, intravenski urogram, intravenski kolangiografija, angiografija i računalna tomografija (CT) s intravaskularnim kontrastnim materijalima) - Studije intravaskularnog kontrasta sa jodirani materijali mogu dovesti do akutne promjene bubrežne funkcije i povezani su s laktacidozom kod bolesnika koji su primali metformin (vidi KONTRAINDIKACIJE). Stoga, u bolesnika kod kojih se planira takva studija, Glucophage ili Glucophage XR treba privremeno prekinuti u vrijeme ili prije postupak i odbijen je 48 sati nakon postupka i ponovno uspostavljen tek nakon što se renalitirana funkcija bubrega i ustanovi da je normalna.
Hipoksična stanja - kardiovaskularni kolaps (šok) iz bilo kojeg razloga, akutno kongestivno zatajenje srca, akutni miokard infarkt i druga stanja karakterizirana hipoksemijom povezana su s mliječnom acidozom i mogu također uzrokovati prerenalna azotemija. Kada se takvi događaji dogode kod pacijenata na terapiji Glucophageom ili Glucophage XR-om, lijek treba odmah prekinuti.
Kirurški zahvati - Glukofage ili Glucophage XR terapiju treba privremeno obustaviti za svaki kirurški postupak (osim manjih postupaka koji nisu povezani s ograničenim unosom hrane i tekućina) i ne treba ga ponovo pokretati sve dok se pacijentov oralni unos ne nastavi i bubrežna funkcija ne ocijeni kao normalna.
Unos alkohola - Poznato je da alkohol pojačava učinak metformina na metabolizam laktata. Stoga bi bolesnike trebalo upozoriti na prekomjerni unos alkohola, akutnog ili kroničnog, dok primaju glukofage ili glukofage XR.
Poremećena jetrena funkcija - Budući da je oslabljena jetrena funkcija povezana s nekim slučajevima laktacidoze, Glukofage i Glucophage XR općenito treba izbjegavati u bolesnika s kliničkim ili laboratorijskim dokazima jetre bolest.
Razina vitamina B12 - u kontroliranim kliničkim ispitivanjima glukofaga u trajanju od 29 tjedana, smanjenje na nenormalne razine prethodno uobičajene razine vitamina B12 u serumu, bez kliničkih manifestacija, zabilježene su u otprilike 7% pacijenata. Takvo smanjenje, možda zbog ometanja apsorpcije B12 iz kompleksa faktora B12-svojstvenog faktora, je, međutim, vrlo rijetko je povezana s anemijom i čini se da je brzo reverzibilna s prestankom uzimanja glukofaga ili vitamina B12 dopunu. Mjerenje hematoloških parametara savjetuje se na pacijentima koji imaju Glucophage ili Glucophage XR na godišnjoj osnovi, a bilo koje prividne nepravilnosti trebaju se na odgovarajući način istražiti i upravljati (vidjeti MJERE OPREZA: Laboratorijski testovi).
Izvjesni pojedinci (oni s nedovoljnim unosom ili apsorpcijom vitamina B12 ili kalcijem) čini se da su skloni razvoju nenormalnih razina vitamina B12. U ovih bolesnika mogu biti korisna rutinska mjerenja vitamina B12 u razmacima od 2 do 3 godine.
Promjena kliničkog statusa bolesnika s prethodno kontroliranim dijabetesom tipa 2 - Pacijent s dijabetesom tipa 2 koji je prethodno bio dobro kontroliran glukofagom ili glukofagom XR razvija laboratorijske abnormalnosti ili kliničku bolest (posebno nejasnu i slabo definiranu bolest), treba odmah ocijeniti zbog dokaza o ketoacidozi ili laktaciji acidoza. Procjena bi trebala uključivati serume elektrolita i ketone, razinu glukoze u krvi i, ako je naznačeno, pH u krvi, laktatu, piruvat i metformin. Ako se pojavi acidoza bilo kojeg oblika, Glucophage ili Glucophage XR moraju se odmah zaustaviti i započeti druge odgovarajuće korektivne mjere (vidjeti također UPOZORENJA).
Hipoglikemija - Hipoglikemija se ne javlja kod pacijenata koji primaju glukofage ili glukofage XR sami u uobičajenim okolnostima upotrebe, ali može se pojaviti kada je unos kalorija nedostatno, ako naporno vježbanje nije nadoknađeno dodatkom kalorija ili tijekom istodobne primjene drugih sredstava za snižavanje glukoze (poput sulfonilureje i inzulina) ili etanol.
Stariji, oslabljeni ili neuhranjeni bolesnici i oni koji imaju insuficijenciju nadbubrežne ili hipofize ili alkoholnu intoksikaciju osobito su osjetljivi na hipoglikemijske učinke. Hipoglikemiju može biti teško prepoznati kod starijih osoba i kod ljudi koji uzimaju lijekove koji blokiraju beta adrenergiku.
Gubitak kontrole glukoze u krvi - Kada je pacijent stabiliziran na bilo kojem režimu dijabetesa izložen stresu poput vrućice, traume, infekcije ili operacije, može doći do privremenog gubitka kontrole glikemije. U takvim bi vremenima moglo biti potrebno odustati od glukofaga ili glukofaga XR i privremeno primijeniti inzulin. Glukofag ili Glucophage XR mogu se vratiti nakon što se akutna epizoda riješi.
Učinkovitost oralnih antidijabetičkih lijekova u snižavanju razine glukoze u krvi kod mnogih bolesnika smanjuje se tijekom vremenskog razdoblja. Ovaj fenomen, koji može biti posljedica progresije osnovne bolesti ili smanjene reakcije na lijek, jest poznat kao sekundarni neuspjeh, za razlikovanje od primarnog neuspjeha u kojem je lijek neučinkovit tijekom početne terapije. Ako dođe do sekundarnog zatajenja ili monoterapijom Glucophage ili Glucophage XR ili sulfonilurejom, kombinirana terapija s Glucophage ili Glucophage XR i sulfonilurejom može rezultirati reakcijom. Ako se dogodi sekundarni zastoj s kombiniranom terapijom glukofagom / sulfonilurejom ili glukofagom Terapija XR / sulfonilurejom, možda će biti potrebno razmotriti terapijske alternative uključujući pokretanje terapija inzulinom.
Informacije za pacijente
Bolesnike treba obavijestiti o potencijalnim rizicima i koristima Glucophagea ili Glucophage XR te alternativnim načinima terapije. Oni bi također trebali biti informirani o važnosti redovitog vježbanja prehrambenih uputa programa i redovitog testiranja glukoze u krvi, glikoziliranog hemoglobina, bubrežne funkcije i hematološkog parametri.
Rizici laktične acidoze, njeni simptomi i stanja koja predisponiraju njen razvoj, kao što je navedeno u UPOZORENJA i MJERE OPREZA odjeljcima, treba objasniti pacijentima. Pacijentima treba savjetovati da odmah prekinu Glucophage ili Glucophage XR i da odmah obavijeste o svom zdravlju praktičar ako neobjašnjiva hiperventilacija, mialgija, neispravnost, neuobičajena somnolencija ili drugi nespecifični simptomi pojaviti. Jednom kada se pacijent stabilizira na bilo kojoj razini doze glukofaga ili glukofaga XR, gastrointestinalni simptomi, koji su uobičajeni tijekom započinjanja terapije metforminom, vjerojatno nisu povezani s lijekom. Kasnija pojava gastrointestinalnih simptoma može biti posljedica laktacidoze ili druge ozbiljne bolesti.
Pacijente treba savjetovati u slučaju prekomjernog unosa alkohola, bilo akutnog ili kroničnog, dok primaju glukofag ili glukofag XR.
Glukofag ili Glucophage XR sami obično ne uzrokuju hipoglikemiju, iako se može pojaviti kada se Glucophage ili Glucophage XR koriste zajedno s oralnim sulfonilureama i inzulinom. Prilikom započinjanja kombinirane terapije, rizika od hipoglikemije, simptoma i liječenja te bolesnici i odgovorna obitelj trebaju objasniti uvjete koji predisponiraju njegov razvoj članovi.
Pacijente treba obavijestiti da glukofage XR moraju progutati cijele, a ne drobiti ih i žvakati, te da neaktivni sastojci mogu se povremeno uklanjati iz izmeta u obliku meke mase koja može nalikovati originalnom tableta.
Laboratorijska ispitivanja
Odgovor na sve dijabetičke terapije treba pratiti periodičnim mjerenjima krvi na testu razina glukoze i glikoziliranog hemoglobina, s ciljem da se te razine smanje na normalne Raspon. Tijekom početne titracije doze, glukoza na glasu može se koristiti za određivanje terapijskog odgovora. Nakon toga treba nadzirati i glukozu i glikozilirani hemoglobin. Mjerenja glikoziliranog hemoglobina mogu biti osobito korisna za procjenu dugoročne kontrole (vidi također DOZIRANJE I UPRAVLJANJE).
Početno i periodično praćenje hematoloških parametara (npr. Hemoglobin / hematokrit i crvena krv stanične indekse) i bubrežnu funkciju (serumski kreatinin) treba izvoditi, barem na godišnjoj osnovi. Iako se megaloblasticanemija rijetko primjećuje uz terapiju glukofagom, ako se sumnja, nedostatak vitamina B12 treba isključiti.
Interakcije lijekova (klinička procjena interakcije lijekova provedenih glukofagom)
Glyburide - U studiji interakcije s jednom dozom bolesnika s dijabetesom tipa 2, istodobna primjena metformin i gliburid nisu rezultirali nikakvim promjenama ni u farmakokinetikama metformina, ni farmakodinamiku. Uočeno je smanjenje AUC i Cmax gliburida, ali vrlo je varijabilno. Priroda pojedinačne doze ovog istraživanja i nedostatak povezanosti između razine gliburida u krvi i farmakodinamičkih učinaka čine klinički značaj ove interakcije neizvjesnim (vidjeti DOZIRANJE I UPRAVLJANJE: Istodobna terapija glukofagom ili glukofagom XR i oralnom sulfonilurejom u odraslih bolesnika).
Furosemid - Ispitivanje interakcije lijekova s jednom dozom metformina i furosemida kod zdravih ispitanika pokazalo je da su istodobnom primjenom farmakokinetičkih parametara oba spoja utjecali. Furosemid je povećao metformin u plazmi i Cmax u krvi za 22%, a AUC u krvi za 15%, bez značajnih promjena u bubrežnom klirensu metformina. Kada su primijenjeni s metforminom, Cmax i AUC furosemida bili su 31% i 12% manji nego tada primijenjeni sami, a terminalni poluživot smanjen je za 32%, bez značajnih promjena u furosemidu bubrega razmak. Nema podataka o interakciji metformina i furosemida ako se primjenjuju istovremeno.
Nifedipin - Studija interakcije lijekova s jednom dozom metformina i nifedipina na normalnim zdravim dobrovoljcima pokazala je da istodobna primjena nifedipina povećala je Cmax i AUC u plazmi za 20%, odnosno 9%, i povećala količinu izlučuje se mokraćom. Tmax i poluživot nisu utjecali. Čini se da nifedipin povećava apsorpciju metformina. Metformin je imao minimalne učinke na nifedipin.
Kationski lijekovi - kationski lijekovi (npr. Amilorid, digoksin, morfin, prokainamid, kinidin, kinin, ranitidin, triamteren, trimetoprim ili vankomicin) koji eliminiraju se putem bubrežne tubularne sekrecije teoretski imaju potencijal interakcije s metforminom natjecajući se za zajednički bubrežni tubulni transport sustavi. Takva interakcija između metformina i oralnog cimetidina zabilježena je kod normalnih zdravih dobrovoljaca i u pojedinačnoj i u više dozi, metformin-cimetidinu studije interakcije lijekova, s povećanjem koncentracije metformina u plazmi i cjelovitom krvnom koncentracijom od 60% i porastom metformina u plazmi i pune krvi AUC. U studiji s jednom dozom nije došlo do promjene poluživota eliminacije. Metformin nije imao utjecaja na farmakokinetiku cimetidina. Iako su takve interakcije i dalje teoretske (osim cimetidina), pažljivo praćenje bolesnika i prilagođavanje doze glukofaga ili glukofaga XR i / ili interferirajući lijek preporučuje se pacijentima koji uzimaju kationske lijekove koji se izlučuju putem proksimalnih bubrežnih tubula sustav.
Ostalo - Neki lijekovi obično stvaraju hiperglikemiju i mogu dovesti do gubitka kontrole glikemije. Ovi lijekovi uključuju tiazide i druge diuretike, kortikosteroide, fenotiazine, štitnjače, estrogeni, oralni kontraceptivi, fenitoin, nikotinska kiselina, simpatomimetici, lijekovi za blokiranje kalcijevih kanala i izoniazid. Kada se takvi lijekovi daju pacijentu koji prima Glucophage ili Glucophage XR, pacijenta treba pomno promatrati zbog gubitka kontrole glukoze u krvi. Kada se takvi lijekovi povuku od pacijenta koji prima Glucophage ili Glucophage XR, pacijenta treba pomno promatrati zbog hipoglikemije.
U zdravih dobrovoljaca farmakokinetika metformina i propranolola, te metformina i ibuprofena nisu utjecala kada su istodobno primijenjeni u ispitivanjima interakcije s jednim dozama.
Metformin se zanemarivo veže na proteine plazme i, stoga je manje vjerovatno da će komunicirati s lijekovima koji su vrlo vezani za proteine poput salicilati, sulfonamidi, kloramfenikol i probenecid, u odnosu na sulfonilureje, koji su jako vezani na serum proteini.
Kancerogeneza, mutageneza, oštećenje plodnosti
Provedena su dugotrajna ispitivanja kancerogenosti na štakorima (trajanje doziranja od 104 tjedna) i miševima (trajanje doziranja od 91 tjedna) u dozama do i uključujući 900 mg / kg / dan i 1500 mg / kg / dan, odnosno. Ove su doze obje približno 4 puta najveće preporučene ljudske dnevne doze od 2000 mg na osnovi usporedbi tjelesne površine. Nisu pronađeni dokazi kancerogenosti metforminom ni kod muških ni kod ženskih miševa. Slično tome, kod mužjaka štakora nije primijećen tumorigenski potencijal sa metforminom. Međutim, povećana je učestalost benignih stromalnih polipa maternice kod ženki štakora liječenih 900 mg / kg / dan.
Nije bilo dokaza o mutagenom potencijalu metformina u sljedećim in vitro testovima: Amesov test (S. typhimurium), test mutacije gena (mišje stanice limfoma) ili test kromosomskih aberacija (humani limfociti). Rezultati ispitivanja in vivo mikronukleusom na mišu također su bili negativni.
Na plodnost mužjaka ili ženki štakora metformin nije utjecao kada su primijenjeni u dozama do 600 mg / kg / dan, što je otprilike 3 puta najveća preporučena dnevna doza za čovjeka na temelju površine tijela usporedbe.
Trudnoća
Teratogeni učinci: Trudnoća kategorija B
Nedavne informacije snažno sugeriraju da su nenormalne razine glukoze u krvi tijekom trudnoće povezane s većom učestalošću urođenih abnormalnosti. Većina stručnjaka preporučuje da se inzulin koristi tijekom trudnoće kako bi se održala razina glukoze u krvi što je moguće bliža normalnoj. Budući da studije reproduktivne reprodukcije na životinjama nisu uvijek prediktivne za odgovor ljudi, Glucophage i Glucophage XR se ne smiju primjenjivati tijekom trudnoće ako to očito nije potrebno.
Ne postoje odgovarajuća i dobro kontrolirana ispitivanja na trudnicama s glukofagom ili glukofagom XR. Metformin nije bio teratogen u štakora i zečeva u dozama do 600 mg / kg / dan. To predstavlja izloženost od oko 2 i 6 puta najveće preporučene dnevne doze od 2000 mg na temelju usporedbe površine tijela za štakore i zečeve. Određivanje fetalnih koncentracija pokazalo je djelomičnu placentarnu barijeru metforminu.
Negovateljice
Studije na dojenim štakorima pokazuju da se metformin izlučuje u mlijeko i dostiže razinu usporedivu s onom u plazmi. Slična ispitivanja nisu provedena i kod dojilja. Budući da potencijal za hipoglikemiju u dojenčadi može postojati, treba donijeti odluku hoće li prekinuti dojenje ili prekinuti lijek, uzimajući u obzir važnost lijeka za majka. Ako se Glukofag ili Glucophage XR prekida i ako sama dijeta nije dovoljna za kontrolu glukoze u krvi, potrebno je razmotriti terapiju inzulinom.
Dječja upotreba
Sigurnost i učinkovitost glukofaga za liječenje dijabetesa tipa 2 utvrđene su u pedijatrijski bolesnici u dobi od 10 do 16 godina (ispitivanja nisu provedena na pedijatrijskim pacijentima mlađim od 10 godina godine). Upotreba glukofaga u ovoj dobnoj skupini potkrijepljena je dokazima iz odgovarajućih i dobro kontroliranih studija glukofaga u odraslih s dodatnim podacima iz kontrolirana klinička studija u pedijatrijskih bolesnika u dobi od 10 do 16 godina s dijabetesom tipa 2, koja je pokazala sličan odgovor u kontroli glikemije kao onaj u odrasli. (Vidjeti KLINIČKA FARMAKOLOGIJA: Pedijatrijske kliničke studije.) U ovoj su studiji štetni učinci bili slični onima opisanim u odraslih. (Vidjeti NEPOVOLJNE REAKCIJE: Pedijatrijski bolesnici.) Preporučuje se maksimalna dnevna doza od 2000 mg. (Vidjeti DOZIRANJE I UPRAVLJANJE: Preporučeni raspored doziranja: Pedijatrija.)
Sigurnost i učinkovitost glukofaga XR u pedijatrijskih bolesnika nisu utvrđene.
Gerijatrijska upotreba
Kontrolirane kliničke studije glukofaga i glukofaga XR nisu uključivale dovoljan broj starijih pacijenata da bi se utvrdilo reagiraju li različito od mlađih bolesnika, mada druga prijavljena klinička iskustva nisu utvrdila razlike u odgovorima između starijih i mlađih pacijenata. Poznato je da se metformin značajno izlučuje putem bubrega i zato što je rizik od ozbiljnih nuspojava na lijek veći u bolesnika s oštećenom funkcijom bubrega, Glucophage i Glucophage XR trebaju se koristiti samo u bolesnika s normalnom funkcijom bubrega (vidjeti KONTRAINDIKACIJE, UPOZORENJA, i KLINIČKA FARMAKOLOGIJA: Farmakokinetika). Budući da je starenje povezano sa smanjenom funkcijom bubrega, Glucophage ili Glucophage XR treba koristiti s oprezom s povećanjem dobi. Treba biti oprezan u odabiru doze, a treba se temeljiti na pažljivom i redovitom praćenju bubrežne funkcije. Općenito, starijim bolesnicima se ne smije titrirati do maksimalne doze glukofaga ili glukofaga XR (vidjeti također UPOZORENJA i DOZIRANJE I UPRAVLJANJE).
vrh
Nuspojave
U američkoj dvostruko slijepoj kliničkoj studiji glukofaga u bolesnika s dijabetesom tipa 2, ukupno 141 pacijent je primio terapiju glukofagom (do 2550 mg dnevno), a 145 bolesnika je dobilo placebo. Nuspojave prijavljene u više od 5% bolesnika sa glukofagom i koje su bile češće u bolesnika liječenih glukofagom nego kod placeba, navedene su u tablici 11.
Tablica 11: Najčešće nuspojave (> 5,0 posto) u placebo kontroliranom kliničkom istraživanju monoterapije glukofagom *
| Negativna reakcija | Glucophage monoterapija (N = 141) |
Placebo (N = 145) |
|---|---|---|
| % bolesnika | ||
| * Reakcije koje su bile češće u bolesnika liječenih glukofagom nego kod placeba. | ||
| Proljev | 53.2 | 11.7 |
| Mučnina / povraćanje | 25.5 | 8.3 |
| Nadutost | 12.1 | 5.5 |
| Astenija | 9.2 | 5.5 |
| loša probava | 7.1 | 4.1 |
| Nelagoda u trbuhu | 6.4 | 4.8 |
| Glavobolja | 5.7 | 4.8 |
Proljev je doveo do prekida ispitivanja lijekova u 6% bolesnika liječenih glukofagom. Pored toga, zabilježene su sljedeće nuspojave kod ¥ ¥ 1,0% do .0 5,0% bolesnika sa glukofagom i češće su prijavljene kod Glucophagea nego placeba: nenormalna stolica, hipoglikemija, mijalgija, vrtoglavica, dispneja, poremećaj noktiju, osip, pojačano znojenje, poremećaj okusa, nelagoda u prsima, zimica, gripu, ispiranje, palpitacije.
U svjetskim kliničkim ispitivanjima, preko 900 bolesnika s dijabetesom tipa 2 liječeno je glukofagom XR u placebo i aktivno kontroliranim studijama. U ispitivanjima koja su kontrolirana placebom, 781 pacijentu je primjenjen Glucophage XR, a 195 bolesnika je dobilo placebo. Nuspojave prijavljene u više od 5% bolesnika Glucophage XR i koje su bile češće u bolesnika liječenih glukofagom XR nego placebo, navedene su u tablici 12.
Tablica 12: Najčešći nuspojave (> 5,0 posto) u placebo kontroliranim studijama glukofaga XR *
| Negativna reakcija | Glukofag XR (N = 781) |
Placebo (N = 195) |
|---|---|---|
| % bolesnika | ||
| * Reakcije koje su bile češće u bolesnika liječenih glukofagom XR nego kod placeba. | ||
| Proljev | 9.6 | 2.6 |
| Mučnina / povraćanje | 6.5 | 1.5 |
Proljev je doveo do prekida ispitivanja lijekova u 0,6% bolesnika liječenih Glucophage XR. Pored toga, slijedeće nuspojave prijavljene su sa ¥ ¥ 1,0% do 5,0% glukofaga XR bolesnika i češće su prijavljene sa Glucophage XR nego placebo: bol u trbuhu, zatvor, zatvor u trbuhu, dispepsija / žgaravica, nadutost, vrtoglavica, glavobolja, gornja respiratorna infekcija, okus poremećaj.
Pedijatrijski bolesnici
U kliničkim ispitivanjima glukofaga u pedijatrijskih bolesnika s dijabetesom tipa 2, profil nuspojava bio je sličan onome opaženom u odraslih.
vrh
Predozirati
Došlo je do predoziranja metformin hidroklorida, uključujući gutanje količine veće od 50 grama. Hipoglikemija je zabilježena u otprilike 10% slučajeva, ali nije utvrđena uzročna povezanost s metformin hidrokloridom. U oko 32% slučajeva predoziranja metforminom zabilježeno je laktacidoza (vidjeti UPOZORENJA). Metformin se može dijalizirati s klirensom do 170 ml / min u dobrim hemodinamičkim uvjetima. Stoga hemodijaliza može biti korisna za uklanjanje nakupljenog lijeka od pacijenata kod kojih se sumnja na predoziranje metforminom.
vrh
Doziranje i primjena
Ne postoji fiksni režim doziranja za liječenje hiperglikemije u bolesnika s dijabetesom tipa 2 s glukofagom ili glukofagom XR ili bilo kojim drugim farmakološkim lijekom. Doziranje glukofaga ili glukofaga XR mora se individualizirati na osnovi učinkovitosti i tolerancije, a ne prekoračiti maksimalne preporučene dnevne doze. Najveća preporučena dnevna doza glukofaga je 2550 mg u odraslih i 2000 mg u pedijatrijskih bolesnika (u dobi od 10-16 godina); maksimalna preporučena dnevna doza glukofaga XR u odraslih je 2000 mg.
Glukofag treba davati podijeljeno u dozi s obrocima, dok se glukofag XR općenito treba davati jednom dnevno uz večernji obrok. Glukofag ili Glucophage XR treba započeti s malom dozom, s postupnim eskalacijom doze, obje za smanjenje gastrointestinalne nuspojave i omogućiti identifikaciju minimalne doze potrebne za odgovarajuću kontrolu glikemije pacijenta.
Tijekom započinjanja liječenja i titracije doze (vidi donju shemu preporučenog doziranja) treba biti glukoza u plazmi na testu koristi se za određivanje terapijskog odgovora na glukofage ili glukofage XR i identificiranje minimalne učinkovite doze za pacijent. Nakon toga, glikozilirani hemoglobin treba izmjeriti u intervalima od približno 3 mjeseca. Terapeutski cilj trebao bi biti smanjenje razine glukoze u plazmi i glikoziliranog nivoa hemoglobina na normalnu ili gotovo normalnu razinu primjenom najniže učinkovite doze glukofaga ili Glucophage XR, bilo kada se koristi kao monoterapija ili u kombinaciji sa sulfonilurejom ili inzulin.
Praćenje glukoze u krvi i glikoziliranog hemoglobina također će omogućiti otkrivanje primarnog zatajenja, tj. Neadekvatno snižavanje glukoze u krvi na maksimalna preporučena doza lijekova i sekundarni neuspjeh, tj. gubitak odgovarajućeg odgovora za snižavanje glukoze u krvi nakon početnog razdoblja učinkovitost.
Kratkotrajna primjena glukofaga ili Glucophage XR može biti dovoljna tijekom razdoblja prolaznog gubitka kontrole kod pacijenata koji su obično dobro kontrolirani samo na dijeti.
Glukofage XR tablete moraju se progutati cijele i nikada ih ne smrviti ili žvakati. Povremeno će se neaktivni sastojci Glucophage XR eliminirati u izmetu kao meka, hidrirana masa.
Preporučeni raspored doziranja
Odrasli
Općenito, klinički značajni odgovori se ne vide kod doza ispod 1500 mg dnevno. Međutim, savjetuje se niža preporučena početna doza i postupno povećana doza kako bi se minimizirali gastrointestinalni simptomi.
Uobičajena početna doza glukofaga (metformin hidroklorid) tablete je 500 mg dva puta dnevno ili 850 mg jednom dnevno, uz obroke. Povećavanje doze trebalo bi biti u koracima od 500 mg tjedno ili 850 mg svaka 2 tjedna, do ukupno 2000 mg dnevno, dano u podijeljenim dozama. Pacijenti se također mogu titrirati od 500 mg dva puta dnevno do 850 mg dva puta dnevno nakon 2 tjedna. Za one bolesnike koji zahtijevaju dodatnu kontrolu glikemije, glukofag se može dati u maksimalnoj dnevnoj dozi od 2550 mg dnevno. Doze veće od 2000 mg mogu se bolje podnijeti tri puta dnevno uz obroke.
Uobičajena početna doza glukofaga XR (metformin hidroklorid) tablete s produljenim oslobađanjem je 500 mg jednom dnevno uz večernji obrok. Povećavanje doze trebalo bi iznositi u obrocima od 500 mg tjedno, do maksimalno 2000 mg jednom dnevno uz večernji obrok. Ako se ne postigne kontrola glikemije na Glucophage XR 2000 mg jednom dnevno, treba razmotriti ispitivanje glukofaga XR 1000 mg dva puta dnevno. Ako su potrebne veće doze metformina, treba koristiti glukofag u ukupnim dnevnim dozama do 2550 mg, davati u podijeljenim dnevnim dozama, kao što je gore opisano. (Vidjeti KLINIČKA FARMAKOLOGIJA: Kliničke studije.)
U randomiziranom ispitivanju, pacijenti koji su trenutno liječeni glukofagom prebačeni su na Glucophage XR. Rezultati ovog ispitivanja pokazuju da se pacijenti koji primaju liječenje glukofagom mogu sigurno prebaciti na Glucophage XR jednom dnevno u istoj dnevnoj dozi, do 2000 mg jednom dnevno. Nakon prelaska s glukofaga na glukofag XR, potrebno je pažljivo nadzirati glikemijsku kontrolu i prilagoditi doziranje u skladu s tim (vidjeti KLINIČKA FARMAKOLOGIJA: Kliničke studije).
pedijatrija
Uobičajena početna doza glukofaga je 500 mg dva puta dnevno, davana uz obroke. Povećavanje doze trebalo bi biti u koracima od 500 mg tjedno do maksimalno 2000 mg dnevno, dano u podijeljenim dozama. Sigurnost i učinkovitost glukofaga XR u pedijatrijskih bolesnika nisu utvrđene.
Prijenos s druge antidijabetičke terapije
Kod prijenosa pacijenata iz standardnih oralnih hipoglikemijskih sredstava koja nisu klorpropamid u glukofage ili glukofage XR općenito nije potrebno prijelazno razdoblje. Kod prijenosa bolesnika s klorpropamida treba biti oprezan tijekom prva 2 tjedna zbog dugotrajno zadržavanje klorpropamida u tijelu, što dovodi do preklapajućeg djelovanja lijekova i moguće hipoglikemije.
Istodobna terapija glukofagom ili glukofagom XR i oralnom sulfonilurejom u odraslih bolesnika
Ako pacijenti nisu odgovorili na 4 tjedna maksimalne doze glukofaga ili Glucophage XR monoterapije, potrebno je razmotriti postupno dodavanje oralna sulfonilureja tijekom nastavka glukofaga ili glukofaga XR u maksimalnoj dozi, čak i ako prethodno ili sekundarno zatajenje sulfonilureje ima dogodila. Podaci o kliničkoj i farmakokinetičkoj interakciji lijeka trenutno su dostupni samo za metformin plus gliburid (glibenklamid).
Uz istodobnu terapiju glukofagom ili glukofagom XR i sulfonilurejom, željena kontrola glukoze u krvi može se postići podešavanjem doze svakog lijeka. U kliničkom ispitivanju bolesnika s dijabetesom tipa 2 i prethodnim neuspjehom na gliburidu, pacijenti su započeli s glukofagom 500 mg, a gliburidom 20 mg titrirano je na 1000/20 mg, 1500/20 mg, 2000/20 mg ili 2500/20 mg glukofaga i gliburida, za postizanje cilja kontrole glikemije, izmjereno FPG, HbA1c i odgovora na glukozu u plazmi (vidjeti KLINIČKA FARMAKOLOGIJA: Kliničke studije). Ipak treba pokušati utvrditi minimalnu učinkovitu dozu svakog lijeka za postizanje tog cilja. Uz istodobnu terapiju glukofagom ili glukofagom XR i sulfonilurejom, rizik od hipoglikemije povezan sa terapijom sulfonilurejom se nastavlja i može se povećati. Treba poduzeti odgovarajuće mjere opreza. (Pogledajte Uložak pakiranja odgovarajuće sulfonilureje.)
Ako pacijenti nisu odgovorili na 1 do 3 mjeseca istodobne terapije s maksimalnom dozom glukofaga ili glukofaga XR i maksimalna doza oralne sulfonilureje, razmotrite terapijske alternative uključujući prelazak na inzulin sa ili bez glukofaga ili glukofaga XR.
Istodobna terapija glukofagom ili glukofagom XR i inzulinom kod odraslih bolesnika
Trenutna doza inzulina treba nastaviti nakon započinjanja terapije glukofagom ili glukofagom XR. Terapija glukofagom ili Glucophage XR treba započeti s 500 mg jednom dnevno kod pacijenata na terapiji inzulinom. Za bolesnike koji ne reagiraju na odgovarajući način, dozu glukofaga ili glukofaga XR treba povećati za 500 mg nakon približno 1 tjedna i nakon toga 500 mg svaki tjedan dok se ne uspostavi odgovarajuća glikemijska kontrola postignut. Maksimalna preporučena dnevna doza je 2500 mg za Glucophage i 2000 mg za Glucophage XR. Preporučuje se da se doza inzulina smanji za 10% do 25% kada se glukoza u plazmi posti koncentracije se smanjuju na manje od 120 mg / dL u bolesnika koji primaju istodobni inzulin i glukofag ili Glukofag XR. Daljnje prilagođavanje treba individualizirati na temelju odgovora za snižavanje glukoze.
Specifične populacije bolesnika
Glukofag ili Glucophage XR se ne preporučuju za upotrebu u trudnoći. Glukofag se ne preporučuje bolesnicima mlađim od 10 godina. Glukofag XR se ne preporučuje u pedijatrijskih bolesnika (mlađih od 17 godina).
Početno i održavajuće doziranje glukofaga ili Glucophage XR trebalo bi biti konzervativno kod bolesnika u poodmakloj dobi zbog potencijala smanjenja bubrežne funkcije u ovoj populaciji. Svako prilagođavanje doze trebalo bi se temeljiti na pažljivoj procjeni bubrežne funkcije. Općenito, stariji, oslabljeni i neuhranjeni bolesnici ne smiju se titrirati do maksimalne doze glukofaga ili glukofaga XR.
Praćenje bubrežne funkcije je neophodno kako bi se pomoglo u prevenciji laktacidoze, osobito u starijih osoba. (Vidjeti UPOZORENJA.)
vrh
Kako se isporučuje
Glucophage® (metformin hidroklorid) Tablete
| 500 mg | Boce od 100 | NDC 0087-6060-05 |
| 500 mg | Boce od 500 | NDC 0087-6060-10 |
| 850 mg | Boce od 100 | NDC 0087-6070-05 |
| 1000 mg | Boce od 100 | NDC 0087-6071-11 |
Glukofage 500 mg tablete su okrugle, bijele do bjelkaste, filmom obložene tablete uklesane s "BMS" 6060 "oko periferije tableta s jedne strane i" 500 "utisnuto preko lica druge strana.
Glukofage 850 mg tablete su okrugle, bijele do gotovo bijele, filmom obložene tablete s dekoltiranim "BMS" 6070 "oko periferije tableta s jedne strane i" 850 "je utisnut preko druge strane strana.
Glukofage 1000 mg tablete su bijele, ovalne, bikonveksne, filmom obložene tablete s "BMS 6071" utisnutim s jedne strane i "1000" s utisnutim na suprotnoj strani i s bisektom s obje strane.
Glucophage® XR (metformin hidroklorid) Tablete s produljenim oslobađanjem
| 500 mg | Boce od 100 | NDC 0087-6063-13 |
| 750 mg | Boce od 100 | NDC 0087-6064-13 |
Glucophage XR tablete od 500 mg bijele su do bjelkaste, bikonveksne tablete u obliku kapsule, s utisnutim "BMS 6063" s jedne strane i "500" utisnutim po licu s druge strane.
Glucophage XR 750 mg tablete su bikonveksne tablete u obliku kapsule, s utisnutim "BMS 6064" s jedne strane, a s druge strane "750". Tablete su blijedo crvene boje i mogu imati pjegav izgled.
skladištenje
Čuvati na 20 ° -25 ° C (68 ° -77 ° F); izleti dopušteni na 15 ° -30 ° C (59 ° -86 ° F). [Pogledajte sobnu temperaturu pod kontrolom USP-a.]
Raspodijelite u posudama otpornim na svjetlost.
Glucophage® je registrirani zaštitni znak tvrtke Merck Santà © S.A.S., suradnika tvrtke Merck KGaA iz Darmstadta, Njemačka. Ima licencu za Bristol-Myers Squibb Company.
Distribuira:
Tvrtka Bristol-Myers Squibb
Princeton, NJ 08543 SAD
zadnje ažuriranje: 01/2009
Glukohage, metformin hidroklorid, podaci o pacijentu (na običnom engleskom)
Detaljne informacije o znakovima, simptomima, uzrocima, liječenjima dijabetesa
Podaci u ovoj monografiji nisu namijenjeni pokrivanju svih mogućih upotreba, uputa, mjera opreza, interakcija s lijekovima ili štetnih učinaka. Ovi podaci su generalizirani i nisu zamišljeni kao posebni medicinski savjeti. Ako imate pitanja o lijekovima koje uzimate ili želite više informacija, obratite se svom liječniku, ljekarniku ili medicinskoj sestri.
natrag na: Pregledajte sve lijekove za dijabetes



